题目内容
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是![]()
![]()
A.![]() 中所含的中子数为
中所含的中子数为![]()
B.36g葡萄糖与果糖的混合物中含有羟基的数目为![]()
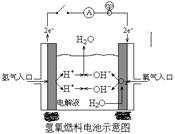
C.用惰性电极电解稀硫酸的过程中,溶液的质量每减少![]() 转移电子数为
转移电子数为![]()
D.![]() 和
和![]() 之和为1mol的
之和为1mol的![]() 溶液中.含有的
溶液中.含有的![]() 数目为
数目为![]()
【答案】B
【解析】
A.![]() 的物质的量为n=
的物质的量为n=![]() =0.2mol,所含中子的数目为
=0.2mol,所含中子的数目为![]() ,故A错误;
,故A错误;
B.葡萄糖和果糖的化学式均为![]() ,故36g混合物的物质的量为
,故36g混合物的物质的量为![]() =0.2mol,1个葡萄糖分子和1个果糖分子中均含5个
=0.2mol,1个葡萄糖分子和1个果糖分子中均含5个![]() ,故
,故![]() 混合物中含有的
混合物中含有的![]() 的个数为
的个数为![]() 个,故
个,故![]() 混合物中含有的
混合物中含有的![]() 的个数为
的个数为![]() 个,故B正确;
个,故B正确;
C.用惰性电极电解稀硫酸,实际电解的物质是水,电解方程式为2H2O![]() 2H2↑+O2↑,每减少2mol水时转移4mol电子,减少
2H2↑+O2↑,每减少2mol水时转移4mol电子,减少![]() 水的物质的量
水的物质的量![]() (H2O)=
(H2O)=![]() =
=![]() =0.2mol,则减少0.2mol水时转移0.4mol电子,电子转移数目为
=0.2mol,则减少0.2mol水时转移0.4mol电子,电子转移数目为![]() ,故C错误;
,故C错误;
D.![]() 溶液中物料守恒关系式为
溶液中物料守恒关系式为![]() ,所以
,所以![]() 和
和![]() 之和为1mol的
之和为1mol的![]() 溶液中,含有的
溶液中,含有的![]() 数目为大于
数目为大于![]() ,故D错误;
,故D错误;
答案选B。

练习册系列答案
相关题目