题目内容
5.下列叙述中,正确的是( )| A. | 在多电子的原子里,能量高的电子通常在离核远的区域内活动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
分析 A、原子核外区域能量不同,离核越近能量越低,离核越远能量越高;
B.根据电子首先进入能量最低、离核最近的轨道判断;
C.微粒可能为不同的分子,也可能为阳离子与阴离子;
D.根据通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构是一种稳定结构.
解答 解:A、原子核外区域能量不同,离核越近能量越低,离核越远能量越高,所以在多电子的原子里,能量高的电子通常在离核远的区域内活动,故A正确;
B.核外电子总是先排在能量低的,但排满了M层的p轨道后就排N层的s轨道,后再排M层的d轨道,不是排满了M层后才排N层,故B错误;
C.微粒可能为不同的分子,也可能为阳离子与阴离子,如钠离子与Ne原子,二者性质不同,故C错误;
D.通常认为最外层有8个电子(最外层是第一电子层时有2个电子)的结构是一种稳定结构,故D错误;
故选:A.
点评 本题考查核外电子排布规律以及元素化学性质和原子构成的关系,要知道电子首先进入能量最低、离核最近的轨道,难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
15.下列各组物质能用分液漏斗分离的是( )
| A. | 苯和甲苯 | B. | 溴和溴苯 | C. | 水和己烷 | D. | 水和乙醛 |
16.下列两种有机物是某些药物中的有效成分:
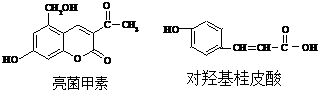
以下说法正确的是( )

以下说法正确的是( )
| A. | 将各1mol的两种物质分别与氢氧化钠溶液充分反应,消耗等量氢氧化钠 | |
| B. | 将各1mol的两种物质分别与溴水充分反应,消耗等量溴分子 | |
| C. | 将各1mol的两种物质分别与氢气充分反应,消耗等量氢气 | |
| D. | 两种有机物中的所有原子均不可能共平面 |
13.下列反应中,起固氮作用的是( )
| A. | NH3经催化氧化生成NO | B. | NO与O2反应生成NO2 | ||
| C. | N2与H2在一定条件下反应生成NH3 | D. | 由NH3制碳酸氢铵和硫酸铵 |
20.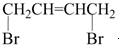 可经三步反应制取
可经三步反应制取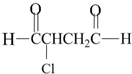 ,发生反应的类型依次是( )
,发生反应的类型依次是( )
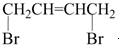 可经三步反应制取
可经三步反应制取 ,发生反应的类型依次是( )
,发生反应的类型依次是( )| A. | 水解反应、加成反应、氧化反应 | B. | 加成反应、水解反应、氧化反应 | ||
| C. | 水解反应、氧化反应、加成反应 | D. | 加成反应、氧化反应、水解反应 |
10.实验室中以下物质的贮存方法,不正确的是( )
| A. | 保存硫酸亚铁溶液时,向其中加入铁钉和少量硫酸 | |
| B. | 少量金属钠保存在煤油中 | |
| C. | 少量液溴可用水封存,防止溴挥发 | |
| D. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
17.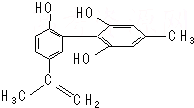 我国支持“人文奥运”,坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”,坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
 我国支持“人文奥运”,坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”,坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 | |
| C. | 该分子中的所有原子有可能共平面 | |
| D. | 1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
14.NOx是大气污染的主要污染物之一.
(1)硝酸厂常用如下三种方法处理氮氧化物(NO与NO2)尾气
①催化还原法:在催化剂存在时用H2将NO2还原为N2,
②Na2CO3溶液吸收法:用Na2CO3溶液吸收NO2生成CO2,若9.2g NO2和Na2CO3溶液完全反应时转移0.1mol电子,则反应的离子方程式为2NO2+CO32-=NO3-+NO2-+CO2.
③烧碱吸收法:氮氧化物(NO与NO2)用烧碱进行吸收,产物为NaNO2、NaNO3和H2O,现有含0.5mol氮氧化物的尾气,恰好被一定体积的25%NaOH溶液(密度1.28g/cm3)完全吸收.已知反应后溶液中含有0.35mo1NaNO2,若将尾气中NO与NO2的平均组成记为NOx,则x=1.8.
(2)现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体在标准状况下的体积与剩余固体的质量如表:
①稀硝酸的浓度为4mol•L-1
②计算原混合物中铁和铜的物质的量比为2:1;
③加入400mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为1.2mol.
(1)硝酸厂常用如下三种方法处理氮氧化物(NO与NO2)尾气
①催化还原法:在催化剂存在时用H2将NO2还原为N2,
②Na2CO3溶液吸收法:用Na2CO3溶液吸收NO2生成CO2,若9.2g NO2和Na2CO3溶液完全反应时转移0.1mol电子,则反应的离子方程式为2NO2+CO32-=NO3-+NO2-+CO2.
③烧碱吸收法:氮氧化物(NO与NO2)用烧碱进行吸收,产物为NaNO2、NaNO3和H2O,现有含0.5mol氮氧化物的尾气,恰好被一定体积的25%NaOH溶液(密度1.28g/cm3)完全吸收.已知反应后溶液中含有0.35mo1NaNO2,若将尾气中NO与NO2的平均组成记为NOx,则x=1.8.
(2)现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体在标准状况下的体积与剩余固体的质量如表:
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 | 8960mL |
②计算原混合物中铁和铜的物质的量比为2:1;
③加入400mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为1.2mol.