题目内容
20.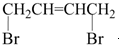 可经三步反应制取
可经三步反应制取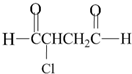 ,发生反应的类型依次是( )
,发生反应的类型依次是( )| A. | 水解反应、加成反应、氧化反应 | B. | 加成反应、水解反应、氧化反应 | ||
| C. | 水解反应、氧化反应、加成反应 | D. | 加成反应、氧化反应、水解反应 |
分析 反应物中含有碳碳双键、溴原子,最终生成物中含有醛基、氯原子,则反应物要采用水解反应将溴原子转化为-OH,采用加成反应将碳碳双键转化为-Cl,最后采用氧化反应将-OH转化为-CHO,据此分析解答.
解答 解:反应物中含有碳碳双键、溴原子,最终生成物中含有醛基、氯原子,则反应物要采用水解反应将溴原子转化为-OH,采用加成反应将碳碳双键转化为-Cl,最后采用氧化反应将-OH转化为-CHO,不能先氧化后加成,因为碳碳双键易被氧化,故选A.
点评 本题考查有机物结构和性质,明确反应前后官能团的变化及官能团变化发生的反应是解本题关键,注意同时含有C=C和-OH时是先发生氧化反应还是先发生加成反应,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列叙述正确的是( )
| A. | 聚丙烯的结构简式为: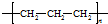 | B. | 氯化氢的电子式为: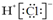 | ||
| C. | 甲烷的比例模型: | D. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl |
11.制备乙酸乙酯的装置如图所示,有关实验室制取乙酸乙酯的说法正确的是( )
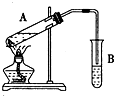

| A. | 试剂添加的顺序为硫酸一乙醇一乙酸 | |
| B. | 无论怎样控制反应条件,1mol乙酸与1mol乙醇反应都不会生成1mol乙酸乙酯 | |
| C. | 试管B中盛有饱和氢氧化钠溶液来除去乙酸乙酯中的杂质,反应后可用分液方法分离 | |
| D. | 生成的乙酸乙酯和硬脂酸甘油酯互为同系物,都可以发生水解反应 |
8.用CH3CO18OH和CH3CH2OH发生酯化反应生成酯A.据此你对该反应所得出的结论是( )
| A. | 生成物中酯A的相对分子质量为88 | |
| B. | 18O全部进入水中 | |
| C. | 18O全部进入生成的酯中 | |
| D. | 酯A与H2O水解后在CH3COOH和CH3CH2OH都有18O存在 |
15.下列物质既能与强酸又能够与强碱反应,且反应后都能产生气体的是( )
| A. | 碳酸氢铵 | B. | 亚硫酸氢钾 | C. | 碳酸氢钠 | D. | 硫酸氢铵 |
5.下列叙述中,正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核远的区域内活动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
12.氨在国防、工农业等领域发挥着重要作用.
(1)工业以甲烷为原料生产氨气的过程如下:甲烷$\stackrel{Ⅰ}{→}$氢气$\stackrel{Ⅱ}{→}$氨气
①过程Ⅰ中,有关化学反应的能量变化如图所示
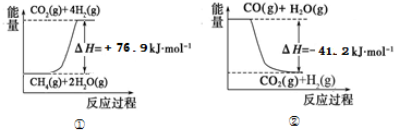
反应①为吸热反应(填“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+118.1KJ/mol.????????
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:
[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g)?[Cu(NH3)2]CH2COO•CO(1),所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是b.(选填字母).
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
⑤下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数
Ⅰ.根据表中数据,得出的结论是氮气和氢气生成氨气的反应是正反应气体体积减小的放热反应.
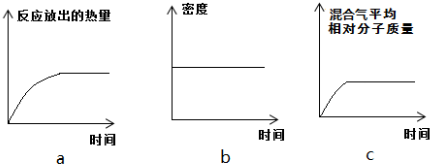
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n(N2)=0.1mol,
n(H2)=0.3mol.下列图象能正确表示该过程中相关量的变化的是ab.(选填字母).
(3)直接供氨式固体氧化物燃料电池能量转化效率达到85%,结构示意图如图:
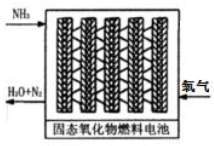
①负极的电极反应式是2NH3-6e-+3O2-=N2+3H2O.
②用该电池电解300moL的饱和食盐水.一段时间后,溶液pH为13(忽略溶液体积的变化),则消耗NH3的体积是0.224L.(标准状况).
(1)工业以甲烷为原料生产氨气的过程如下:甲烷$\stackrel{Ⅰ}{→}$氢气$\stackrel{Ⅱ}{→}$氨气
①过程Ⅰ中,有关化学反应的能量变化如图所示

反应①为吸热反应(填“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+118.1KJ/mol.????????
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:
[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g)?[Cu(NH3)2]CH2COO•CO(1),所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是b.(选填字母).
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
⑤下表是过程Ⅱ中,反应物的量相同时,不同条件下平衡体系中氨的体积分数
 | 15.2MPa | 20.3MPa | 30.4MPa |
| 400℃ | 32.8% | 38.8% | 48.2% |
| 450℃ | 22.4% | 27.5% | 35.9% |
| 500℃ | 14.9% | 18.8% | 25.8 |
Ⅱ.恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡时n(N2)=0.1mol,
n(H2)=0.3mol.下列图象能正确表示该过程中相关量的变化的是ab.(选填字母).

(3)直接供氨式固体氧化物燃料电池能量转化效率达到85%,结构示意图如图:

①负极的电极反应式是2NH3-6e-+3O2-=N2+3H2O.
②用该电池电解300moL的饱和食盐水.一段时间后,溶液pH为13(忽略溶液体积的变化),则消耗NH3的体积是0.224L.(标准状况).
10.23Na与23Na+比较,相同的是( )
| A. | 微粒半径 | B. | 化学性质 | C. | 最外层电子数 | D. | 质子数 |