题目内容
16.下列两种有机物是某些药物中的有效成分: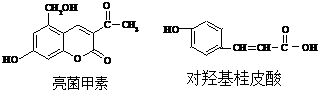
以下说法正确的是( )
| A. | 将各1mol的两种物质分别与氢氧化钠溶液充分反应,消耗等量氢氧化钠 | |
| B. | 将各1mol的两种物质分别与溴水充分反应,消耗等量溴分子 | |
| C. | 将各1mol的两种物质分别与氢气充分反应,消耗等量氢气 | |
| D. | 两种有机物中的所有原子均不可能共平面 |
分析 亮菌甲素含有酚羟基,可发生取代、显色和氧化反应,含有醇羟基,可发生取代、氧化反应,含有酯基,可发生取代反应,含有碳碳双键,可发生加成、加聚和氧化反应,含有羰基,可发生加成反应,对羟基桂皮酸含有酚羟基,可发生取代、显色和氧化反应,含有碳碳双键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化反应,以此解答.
解答 解:A.亮菌甲素中能与氢氧化钠反应的官能团为酚羟基和酯基,且酯基水解生成酚羟基,则1mol亮菌甲素可消耗3mol氢氧化钠,而对羟基桂皮酸中能与氢氧化钠反应的官能团为酚羟基和羧基,1mol对羟基桂皮酸可消耗2mol氢氧化钠,故A错误;
B.两种有机物都含有酚羟基,且可被溴取代邻位氢原子,都含有碳碳双键,可与溴发生加成反应,则将各1mol的两种物质分别与溴水充分反应,消耗等量溴分子,故B正确;
C.亮菌甲素中能与氢气反应的官能团为苯环、碳碳双键和羰基,对羟基桂皮酸中能与氢气发生加成反应的官能团为苯环和碳碳双键,消耗氢气的量不等,故C错误;
D.对羟基桂皮酸含有苯环、碳碳双键和羧基,具有苯、乙烯和甲醛的平面形结构特点,所用的原子可在同一个平面上,故D错误.
故选B.
点评 本题考查有机物的结构与性质,为高考常见题型,注意把握有机物官能团与性质的关系来解答,熟悉酚、酯、烯烃的性质是解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.近日,我国不少城市出现了罕见的连续雾霾天气,导致当下雾霾天气的主要原因是化石燃料的大量使用,下列与治理雾霾天气的相关说法不正确的是( )
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发新能源,如太阳能、风能等,减少对化石能源的依赖 | |
| C. | 在汽车尾气处理器中使用新的催化剂,促使汽车尾气中CO和NO转化为无污染物 | |
| D. | 化石燃料燃烧产生的CO2、SO2、NO2都会导致酸雨的形成 |
7.下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题.
(1)在这10种元素中,化学性质最不活泼的是⑩(写序号),失电子能力最强的原子是K(用元素符号表示).
(2)在这10种元素中,最高价氧化物的水化物碱性最强的是KOH(填化学式),最高价氧化物的水化物酸性最强的是HClO4(填化学式).
(3)H分别与④、⑤、⑦、⑧、⑨形成的化合物中,最稳定的是HF(填化学式);
(4)①、⑧、⑨三种元素单核离子半径由小到大的顺序是(用相应的离子符号表示):Na+<F-<Cl-
(5)写出③和⑨形成的化合物的电子式: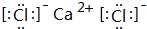 ,化学键类型为离子键(“离子键”或“共价键”).
,化学键类型为离子键(“离子键”或“共价键”).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑧ | ⑩ | |||
| 3 | ① | ⑦ | ⑨ | |||||
| 4 | ② | ③ |
(2)在这10种元素中,最高价氧化物的水化物碱性最强的是KOH(填化学式),最高价氧化物的水化物酸性最强的是HClO4(填化学式).
(3)H分别与④、⑤、⑦、⑧、⑨形成的化合物中,最稳定的是HF(填化学式);
(4)①、⑧、⑨三种元素单核离子半径由小到大的顺序是(用相应的离子符号表示):Na+<F-<Cl-
(5)写出③和⑨形成的化合物的电子式:
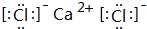 ,化学键类型为离子键(“离子键”或“共价键”).
,化学键类型为离子键(“离子键”或“共价键”).
4.下列判断错误的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 沸点:H2O<H2S<H2Se | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 熔点:金刚石>NaCl>冰 |
11.制备乙酸乙酯的装置如图所示,有关实验室制取乙酸乙酯的说法正确的是( )


| A. | 试剂添加的顺序为硫酸一乙醇一乙酸 | |
| B. | 无论怎样控制反应条件,1mol乙酸与1mol乙醇反应都不会生成1mol乙酸乙酯 | |
| C. | 试管B中盛有饱和氢氧化钠溶液来除去乙酸乙酯中的杂质,反应后可用分液方法分离 | |
| D. | 生成的乙酸乙酯和硬脂酸甘油酯互为同系物,都可以发生水解反应 |
1.下列物质中既不是同系物,也不是同分异构体,但最简式相同的是( )
| A. | CH3CH=CH2和 | B. | 乙炔和苯 | C. |  和 和 | D. | 葡萄糖与麦芽糖 |
8.用CH3CO18OH和CH3CH2OH发生酯化反应生成酯A.据此你对该反应所得出的结论是( )
| A. | 生成物中酯A的相对分子质量为88 | |
| B. | 18O全部进入水中 | |
| C. | 18O全部进入生成的酯中 | |
| D. | 酯A与H2O水解后在CH3COOH和CH3CH2OH都有18O存在 |
5.下列叙述中,正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核远的区域内活动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
 ③2-甲基-1-戊烯:CH2=CH(CH3)CH2CH2CH3
③2-甲基-1-戊烯:CH2=CH(CH3)CH2CH2CH3