题目内容
9. 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量•
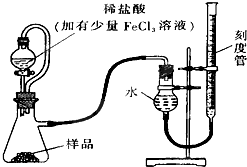
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量•(1)某研究小组拟用如图装置测定一定质量的样品中过氧化镁的含量.
①实验开始之前应该检查装置的气密性稀盐酸中加入少量FeCl3溶液的作用是用作催化剂(或催化H2O2的分解).MgO2的电子式为

②实验结束后,待恢复至室温,将右侧刻度管缓缓向下移动直到两侧液面相平,再平视刻度线读数.
(2)实验室还可通过以下方案测定样品中过氧化镁的含量:取a g样品,加入足量稀盐酸,充分反应后再加入NaOH溶液至Mg2+沉淀完全,过滤、洗涤后,将滤渣充分灼烧,最终得到b g固体.已知:常温下Ksp[Mg(OH)2]=1×10-11.为使溶液中的Mg2+完全沉淀[即溶液中c(Mg2+)≤1×10-5mol/L],溶液的pH至少应调至11.则样品中过氧化镁的质量分数为$\frac{7(a-b)}{2a}$ (用含a、b的表达式表示).
(3)实验室中某含Mg2+的溶液中混有Fe3+,可用Mg(OH)2调溶液PH值除去Fe3+,写出该沉淀转化反应的离子方程式3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3.
分析 (1)①实验前需进行的操作是检查装置的气密性;通过测量双氧水分解生成的氧气,可检测过氧化镁的含量,而氯化铁能作催化剂加快双氧水的分解,加快反应速率,过氧化镁是离子化合物,据此写出电子式;
(2)根据氢氧化镁的溶度积,计算出溶液中氢氧根离子的浓度,求出溶液的PH;质量b是氧化镁,质量a是过氧化镁和氧化镁杂质质量,设出二者物质的量,列式计算出各自物质的量,最后根据过氧化镁的物质的量,算出其质量分数;
(3)用Mg(OH)2调溶液PH值除去Fe3+,利用氢氧化镁和溶液中氢离子反应促进铁离子水解正向进行,生成氢氧化铁沉淀.
解答 解:(1)①实验装置连接好以后,实验前需进行的操作是检查装置的气密性;过氧化镁溶于水生成双氧水,双氧水易分解,通过测量双氧水分解生成的氧气,可检测过氧化镁的含量,而氯化铁能作催化剂加快双氧水的分解,加快反应速率,过氧化镁是离子化合物,其电子式为 ,
,
故答案为:检查装置的气密性;用作催化剂(或催化H2O2的分解); ;
;
(2)根据氢氧化镁的溶度积常数可知,当溶液中c(Mg2+)=l×10-5mol/L时,Ksp[Mg(OH)2]=1×10-11=c(Mg2+)•c2(OH-),溶液中OH-浓度等于1×10-3mol/L,所以溶液的pH=11;
设过氧化镁的物质的量是xmol,氧化镁物质的量是ymol,则56x+40y=a,(x+y)×40=b,解得x=$\frac{a-b}{16}$,方案I中过氧化镁的质量分数为:$\frac{\frac{a-b}{16}×56}{a}$=$\frac{7(a-b)}{2a}$,
故答案是:11; $\frac{7(a-b)}{2a}$;
(3)用Mg(OH)2调溶液PH值除去Fe3+,利用氢氧化镁和溶液中氢离子反应促进铁离子水解正向进行,生成氢氧化铁沉淀,反应的;离子方程式为:3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3,故答案为:3Mg(OH)2+2Fe3+=3Mg2++2Fe(OH)3.
点评 该题是高考中的常见题型,属于中等难度的试题,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生规范严谨的实验设计、操作能力;该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力.

| A. | 电解池的阳极发生氧化反应,阴极上发生还原反应 | |
| B. | 不能自发进行的氧化还原反应可通过电解的原理实现 | |
| C. | 电镀时,电镀池里的阳极材料发生氧化反应 | |
| D. | 电解饱和食盐水时,阳极得到,NaOH溶液和氢气 |
| A. | 1 mol氧的质量为32g | |
| B. | 标准状况下,0.5 mol NO和0.5 mol O2的混合气体体积约为22.4L | |
| C. | CO2的摩尔质量为44g/mol | |
| D. | 1L 2 mol/L的BaCl2溶液中含Cl-的个数为2.408×1024 |
| A. | 甲烷和乙烷 | B. | O2和O3 | C. | 12C和14C | D. | 正丁烷和异丁烷 |
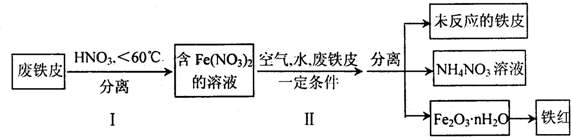
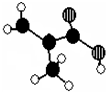
 ,W是否存在顺反异构?否 (填“是”或“否”).
,W是否存在顺反异构?否 (填“是”或“否”).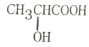 是W与水在一定条件下发生加成反应的产物的同系物.
是W与水在一定条件下发生加成反应的产物的同系物.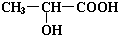 +2Na→
+2Na→ +H2↑.
+H2↑.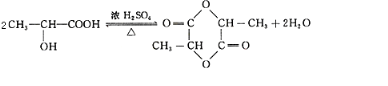 .
.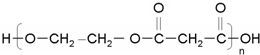 的单体:乙二醇、丙二酸.
的单体:乙二醇、丙二酸.