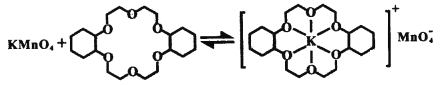
题目内容
【题目】常温下,下列说法正确的是( )
A. 取等体积、同浓度的醋酸和盐酸溶液与足量Zn反应,产生的氢气量一样多。
B. 用HF溶液做导电性实验,灯泡很暗,则一定说明HF为弱电解质。
C. 稀释醋酸溶液,溶液中所有离子浓度都减少。
D. 氨水稀释时,![]() 不断减少
不断减少
【答案】A
【解析】
A.酸与足量的锌反应生成氢气的量与氢离子的物质的量成正比,体积相等、浓度相等的盐酸与醋酸溶液中氢离子的物质的量相等,所以与足量锌完全反应时生成的氢气的量一样多,故A正确;
B.用HF溶液做导电性实验,灯泡很暗,说明该溶液中离子浓度较小,但不能说明HF部分电离,可能是因为HF的浓度很小,则不能证明HF是弱酸,故B错误;
C.加水稀释醋酸,溶液中的c(CH3COOH)、c(CH3COO-)、c(H+)均降低,但由于Kw不变,故溶液中的c(OH-)增大,故C错误;
D.加水稀释过程中促进一水合氨电离,则n(NH4+)增大、n(NH3H2O)减小,![]() =
=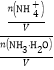 =
=![]() 增大,故D错误;
增大,故D错误;
答案选A。

【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)原子半径最小的元素是___(填元素名称),写出⑥的离子结构示意图___。
(2)③的单质的电子式为__。
(3)以上9种元素中最高价氧化物对应水化物酸性最强的是___(填化学式)。
(4)⑤与⑦形成的化合物中,化学键类型为___。
(5)②与④形成的原子个数比为1:2的化合物的结构式为____。
(6)③、④、⑥的原子半径由大到小的顺序为___(用元素符号回答)。
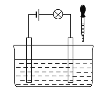
(7)为探究元素②和⑧的非金属性强弱,某同学设计了如图所示的装置进行实验(夹持仪器已略去,装置气密性良好)。请回答:
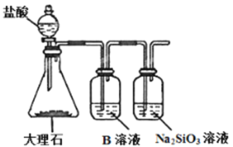
a.溶液B的作用是___。
b.上述实验中,能说明②和⑧非金属性强弱的化学方程式是___。
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向KI溶液中滴入少量新制氯水和四氯化碳,振荡、静置,溶液下层呈紫红色 | I的还原性强于Cl |
B | 向无水乙醇中加入浓H2SO4,加热,将产生的气体通入酸性KMnO4溶液,紫红色褪去 | 该气体一定是乙烯 |
C | 测定Na2CO3和Na2SiO3溶液的pH,后者pH比前者的大 | C的非金属性比Si强 |
D | 向1-溴丙烷中加入KOH溶液,加热几分钟,冷却后再加入AgNO3溶液,无淡黄色沉淀生成 | 1-溴丙烷没有水解 |
A.AB.BC.CD.D