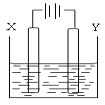
题目内容
【题目】海水晒盐得到的粗盐中还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是实验室制备精盐的实验方案:

(1)除去泥沙和沉淀选用图中___装置,B装置的操作名称是___,在上述方案中图中装置中不会用到的是___。
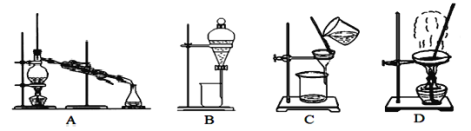
(2)第⑦步操作的名称是___,所用到的实验装置是图中的___(填字母);
(3)为除去粗盐中的可溶性杂质,通常采用以下三种试剂,a:Na2CO3溶液;b:BaCl2溶液;c:NaOH溶液,加入BaCl2试剂的目的是___,三种试剂加入的合理顺序是___。
【答案】C 分液 A、B 蒸发结晶 D 除去Na2SO4(或除去SO42-) cba(bca)
【解析】
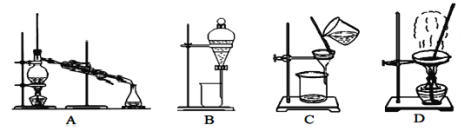
A装置为蒸馏装置,用于分离沸点相差较大的液体混合物;B装置为分液装置,用于分离不互溶的液体混合物;C装置为过滤装置,用于分离混有固、液混合物;D装置为蒸发装置,用于从溶液中提取溶质溶液。
从实验流程图看,各步操作的目的是:①溶解粗盐,②、③、④除去粗盐中的CaCl2、MgCl2、Na2SO4杂质,⑤去除盐水中的难溶性杂质,⑥除去食盐水中的Na2CO3和NaOH杂质,⑦提取精盐水中的NaCl。
(1)从粗盐水中去除泥沙和沉淀,属于固、液混合物的分离,选用图中C装置。答案为C;
B装置的操作名称是分液。答案为分液;
在上述方案中,不会用到的是图中的蒸馏装置和分液装置。答案为A、B;
(2)第⑦步操作的目的是提取精盐水中的NaCl,所以操作名称是蒸发结晶。答案为蒸发结晶
所用到的实验装置是图中的D。答案为D;
(3)为除去粗盐中的可溶性杂质,通常采用以下三种试剂,a:Na2CO3溶液;b:BaCl2溶液;c:NaOH溶液,加入BaCl2试剂的目的是除去Na2SO4(或除去SO42-)。
答案为:除去Na2SO4(或除去SO42-);
因为加入的除杂试剂都是过量的,过量的除杂试剂也将成为杂质,需要去除。BaCl2过量时,只能用Na2CO3除去,所以Na2CO3一定要在BaCl2之后加入。因此三种试剂加入的合理顺序是cba(bca)。答案为cba(bca)。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】海水中有丰富的资源,多种多样的海洋动物、植物、矿藏等。如图是从海水中提取某些物质的示意图。已知:海水中含量最高的几种离子的浓度依次为
微粒种类 | Cl- | Na+ | Mg2+ |
| Ca2+ |
微粒浓度 | 0.55mol·L-1 | 0.47mol·L-1 | 0.054mol·L-1 | 0.027mol·L-1 | 0.01mol·L-1 |
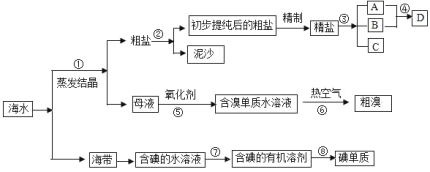
请根据以上信息回答下列问题:
(1)写出步骤②的操作名称_______;实验室中步骤⑤所需的玻璃仪器除烧杯外,还需要的仪器是___________。
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式___________。
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、![]() 等杂质,精制得到精盐的步骤顺序为________。(用字母序号填空)
等杂质,精制得到精盐的步骤顺序为________。(用字母序号填空)
a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)____________(填“能”或“不能”)用![]() 一种试剂替代步骤②中两种试剂,理由是________。
一种试剂替代步骤②中两种试剂,理由是________。