题目内容
【题目】汽车排放的尾气是大气污染气体之一。如何减少污染气体的排放是科学家研究的热门课题。请回答下列问题:
(1)已知:CO的燃烧热为283.0kJ·mol1,N2(g)+2O2(g) =2NO2(g) ΔH=+64kJ·mol1,则NO2(g)+2CO(g)=![]() N2(g)+2CO2(g) ΔH=___kJ·mol1,若反应中有14g还原剂发生反应,则转移电子___mol。
N2(g)+2CO2(g) ΔH=___kJ·mol1,若反应中有14g还原剂发生反应,则转移电子___mol。
(2)使汽车排放的CO和NO在一定条件下发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
N2(g)+2CO2(g),可有效地减少空气污染。若在一定温度下,将6molNO、8molCO充入10L固定容积的容器中发生上述反应,反应过程中各物质的浓度变化如图1所示。
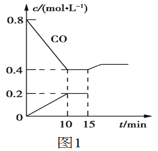
①该反应的化学平衡常数K=___。NO的平衡转化率=___。
②15min时,若改变反应条件,导致CO浓度发生如图1所示的变化,则改变的条件可能是___。
a.缩小容器体积b.增加CO2的量c.体积不变通入少量氩气d.加入催化剂
③当NO与CO的起始浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图2所示,则下列说法正确的是___。
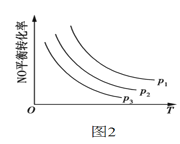
A.该反应ΔH<0 B.p1<p2<p3
C.升高温度正反应速率减小,逆反应速率增大 D.温度不变,增大压强,平衡常数增大
④以下说法中能判断反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)达到平衡的是___。
N2(g)+2CO2(g)达到平衡的是___。
A.反应物和生成物的物质的量相等 B.单位时间内消耗1molNO同时生成1molCO2
C.混合气体压强不再发生变化 D.NO的浓度不再变化
⑤向反应容器中再分别充入下列气体,能使NO转化率增大的是___。
A.O2 B.N2 C.CO D.NO
【答案】-598 1 5 66.7% ab A C、D C
【解析】
(1)①N2(g)+2O2(g) ![]() 2NO2(g) ΔH=+64kJ·mol1;CO的燃烧热为283.0kJ·mol1则②CO(g)+
2NO2(g) ΔH=+64kJ·mol1;CO的燃烧热为283.0kJ·mol1则②CO(g)+ ![]() O2(g)=CO2(g) ΔH= -283.0kJ·mol1;②×2-
O2(g)=CO2(g) ΔH= -283.0kJ·mol1;②×2-![]() ×①得NO2(g)+2CO(g)=
×①得NO2(g)+2CO(g)=![]() N2(g)+2CO2(g);
N2(g)+2CO2(g);
(2)①列方程式的“三段式”根据公式K=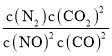 可以求得;
可以求得;
②由图可知15min时CO的浓度增加并且反应速率比0-10min小,说明反应左移且没有增加反应速率;
③A. 由图可知,升高温度,NO的平衡转化率减小,反应左移,说明该反应放热,ΔH<0,故A正确;
B. 反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)是气体体积减小的反应,增大压强反应右移,NO的平衡转化率增大,由图可知平衡转化率:p1>p2>p3,则压强关系:p1>p2>p3,故B错误;
N2(g)+2CO2(g)是气体体积减小的反应,增大压强反应右移,NO的平衡转化率增大,由图可知平衡转化率:p1>p2>p3,则压强关系:p1>p2>p3,故B错误;
C. 升高温度正反应速率和逆反应速率都增大,故C错误;
D. 平衡常数和温度有关,温度不变,平衡常数不变,故D错误;
④根据反应到达平衡的条件判断;
⑤使NO转化率增大即反应右移。
(1)①N2(g)+2O2(g) ![]() 2NO2(g) ΔH=+64kJ·mol1;CO的燃烧热为283.0kJ·mol1则②CO(g)+
2NO2(g) ΔH=+64kJ·mol1;CO的燃烧热为283.0kJ·mol1则②CO(g)+ ![]() O2(g)=CO2(g) ΔH= -283.0kJ·mol1;②×2-
O2(g)=CO2(g) ΔH= -283.0kJ·mol1;②×2-![]() ×①得NO2(g)+2CO(g)=
×①得NO2(g)+2CO(g)=![]() N2(g)+2CO2(g) ΔH= -283.0kJ·mol1×2-64×
N2(g)+2CO2(g) ΔH= -283.0kJ·mol1×2-64×![]() kJ·mol1= -598 kJ·mol1;该反应中还原剂是CO,C元素从+2价变成+4价,转移2个电子,14gCO的物质的量是
kJ·mol1= -598 kJ·mol1;该反应中还原剂是CO,C元素从+2价变成+4价,转移2个电子,14gCO的物质的量是![]() =0.5mol,共转移电子0.5mol×2=1mol;
=0.5mol,共转移电子0.5mol×2=1mol;
(2)①2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始(mol/L)0.6 0.8 0 0
转化(mol/L)0.4 0.4 0.2 0.4
平衡(mol/L)0.2 0.4 0.2 0.4
K=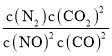 =
=![]() =5;NO的平衡转化率=
=5;NO的平衡转化率=![]() ×100%=66.7%;
×100%=66.7%;
②由图可知15min时CO的浓度增加并且反应速率比0-10min小,说明反应左移且没有增加反应速率,反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)是气体体积减小的反应,所以减小压强或者增加CO2的量可以让反应左移,故选ab;
N2(g)+2CO2(g)是气体体积减小的反应,所以减小压强或者增加CO2的量可以让反应左移,故选ab;
③A. 由图可知,升高温度,NO的平衡转化率减小,反应左移,说明该反应放热,ΔH<0,故A正确;
B. 反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)是气体体积减小的反应,增大压强反应右移,NO的平衡转化率增大,由图可知平衡转化率:p1>p2>p3,则压强关系:p1>p2>p3,故B错误;
N2(g)+2CO2(g)是气体体积减小的反应,增大压强反应右移,NO的平衡转化率增大,由图可知平衡转化率:p1>p2>p3,则压强关系:p1>p2>p3,故B错误;
C. 升高温度正反应速率和逆反应速率都增大,故C错误;
D. 平衡常数和温度有关,温度不变,平衡常数不变,故D错误;
故选A;
④A. 反应物和生成物的物质的量相等不能说明反应已经到达平衡,故A错误;B. 单位时间内消耗1molNO同时生成1molCO2,则V正(NO)= 2V正(CO2),不能说明反应到达平衡,故B错误;C. 反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)是气体体积减小的反应,混合气体压强不再发生变化,则气体体积不再变化,说明反应到达平衡,故C正确;D. NO的浓度不再变化说明反应到达平衡,故D正确;故选CD;
N2(g)+2CO2(g)是气体体积减小的反应,混合气体压强不再发生变化,则气体体积不再变化,说明反应到达平衡,故C正确;D. NO的浓度不再变化说明反应到达平衡,故D正确;故选CD;
⑤使NO转化率增大即反应右移,需要加入反应物CO,加入NO等效于增大压强,反应左移NO转化率减小,故选C。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案