题目内容
某温度(T℃)时,测得0.01mol?L-1 NaOH溶液的pH=11,则该温度下水的Kw= .在此温度下,将
pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合.
(1)若所得混合液为中性,且a=11,b=3,则Va:Vb= .
(2)若所得混合液的pH=10,且a=12,b=2,则Va:Vb= .
pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合.
(1)若所得混合液为中性,且a=11,b=3,则Va:Vb=
(2)若所得混合液的pH=10,且a=12,b=2,则Va:Vb=
考点:pH的简单计算,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)0.01mol/L的NaOH溶液的pH为11,则c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,根据Kw=c(H+)×c(OH-)计算;
(2)将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合,
①若所得混合溶液为中性,且a=11,b=3,根据c(OH-)×Va=c(H+)×Vb计算;
②若所得混合溶液的pH=10,碱过量,计算出c(OH-)与酸碱的物质的量的关系,可计算.
(2)将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合,
①若所得混合溶液为中性,且a=11,b=3,根据c(OH-)×Va=c(H+)×Vb计算;
②若所得混合溶液的pH=10,碱过量,计算出c(OH-)与酸碱的物质的量的关系,可计算.
解答:
解:(1)0.01mol/L的NaOH溶液的pH为11,则c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,Kw=c(H+)×c(OH-)=1×10-13,
故答案为:1×10-13;
(2)将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合,
①若所得混合溶液为中性,且a=11,b=3,因c(OH-)×Va=c(H+)×Vb,a=11,溶液中氢氧根离子浓度为0.01mol/L,b=3,则氢离子浓度为0.001mol/L,则0.01×Va=0.001Vb,则Va:Vb=1:10,
故答案为:1:10;
②若所得混合溶液的pH=10,混合液中碱过量,该温度下氢氧根离子浓度为0.001mo/L,a=12,氢氧根离子浓度为0.1mol/L,b=2,溶液中氢离子浓度为0.01mol/L,则c(OH-)=
=0.001mol/L,
解得:Va:Vb=1:9,
故答案为:1:9.
故答案为:1×10-13;
(2)将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合,
①若所得混合溶液为中性,且a=11,b=3,因c(OH-)×Va=c(H+)×Vb,a=11,溶液中氢氧根离子浓度为0.01mol/L,b=3,则氢离子浓度为0.001mol/L,则0.01×Va=0.001Vb,则Va:Vb=1:10,
故答案为:1:10;
②若所得混合溶液的pH=10,混合液中碱过量,该温度下氢氧根离子浓度为0.001mo/L,a=12,氢氧根离子浓度为0.1mol/L,b=2,溶液中氢离子浓度为0.01mol/L,则c(OH-)=
| 0.1Va-0.01Vb |
| Va+Vb |
解得:Va:Vb=1:9,
故答案为:1:9.
点评:本题考查酸碱混合的计算,明确该温度下的Kw及pH与浓度的换算是解答本题的关键,注意酸碱反应的实质即可解答,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、金属钠着火可用煤油扑灭 |
| B、将几滴FeCl3饱和溶液滴入氢氧化钠溶液可制备Fe(OH)3胶体 |
| C、向含有等量NaI、NaCl的溶液中滴加AgNO3溶液,先产生白色沉淀 |
| D、用浓氢氧化钠溶液和湿润红色石蕊试纸检验某溶液中是否有NH4+ |
铅蓄电池在日常生活中有着广泛的应用,它的电池反应为Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列说法正确的是( )
| A、正极反应为:Pb+SO42--2e-═PbSO4 |
| B、负极反应为:PbO2+SO42-+4H++2e-═PbSO4+2H2O |
| C、随着电池的工作,电解质溶液中H2SO4的浓度逐渐降低 |
| D、随着电池的工作,负极区的pH减小 |
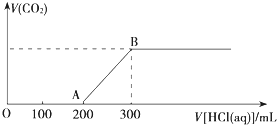 向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7. 根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.
根据氧化还原反应:Zn(s)+2Ag+(aq)═Zn2+(aq)+2Ag(s),试设计一个简单的原电池.