题目内容
写出下列物质在水溶液里的电离方程式:
(1)硫酸铁 ;
(2)氢氧化铝 ;
(3)硫酸氢钾 .
(1)硫酸铁
(2)氢氧化铝
(3)硫酸氢钾
考点:离子方程式的书写
专题:离子反应专题
分析:根据所给电解质的组成微粒分析电解后的离子,然后依据电离方程式的书写规则进行书写,强电解质写“=”、弱电解质写“?”,且要遵循原子守恒、电荷守恒.
解答:
解:(1)硫酸铁电离后生成铁离子和硫酸根离子,电离方程式为Fe2(SO4)3=2Fe3++3SO42-,故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(2)氢氧化铝电离后生成铝离子和氢氧根离子,电离方程式为Al(OH)3?Al3++3OH-,故答案为:Al(OH)3?Al3++3OH-;
(3)硫酸氢钾电离后生成钾离子、氢离子和硫酸根离子,电离方程式为:KHSO4=K++H++SO42-,故答案为:KHSO4=K++H++SO42-.
(2)氢氧化铝电离后生成铝离子和氢氧根离子,电离方程式为Al(OH)3?Al3++3OH-,故答案为:Al(OH)3?Al3++3OH-;
(3)硫酸氢钾电离后生成钾离子、氢离子和硫酸根离子,电离方程式为:KHSO4=K++H++SO42-,故答案为:KHSO4=K++H++SO42-.
点评:在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写离子方程式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对于可逆反应H2(g)+I2(g)?2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A、H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B、若平衡正向移动,则V正一定增大 |
| C、正、逆反应速率的比值是恒定的 |
| D、达到平衡时,正、逆反应速率相等 |
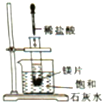 如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.下列说法不正确的是( )
如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.下列说法不正确的是( )| A、试管中有气泡产生 |
| B、烧杯内出现浑浊 |
| C、镁条的化学能大于氢气 |
| D、镁条与稀盐酸的反应为放热反应 |
 2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物.已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想.运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物.已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键.