题目内容
某学生用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
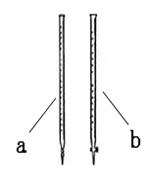
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。回答下列问题:
(1)正确的操作顺序是:B、 、F(填序号);
(2)上述B步骤操作的目的是 ;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响
是 (填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是 ;
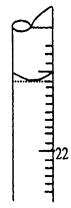
(5)若滴定结束时,滴定管液面如图所示,则终点读数为 mL。
(6)根据读数计算出该待测液的浓度为 。
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。回答下列问题:

(1)正确的操作顺序是:B、 、F(填序号);
(2)上述B步骤操作的目的是 ;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响
是 (填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是 ;
(5)若滴定结束时,滴定管液面如图所示,则终点读数为 mL。
(6)根据读数计算出该待测液的浓度为 。
(1)D C E A (2)防止滴定管内壁附着的水将标准溶液稀释而带来误差
(3)偏大 (4)溶液由无色变为浅红色,且半分钟内不褪色
(5)21.10 (6)0.09000mol·L-1
(3)偏大 (4)溶液由无色变为浅红色,且半分钟内不褪色
(5)21.10 (6)0.09000mol·L-1
试题分析:(1)用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液时,其正确的操作为用标准氢氧化钠溶液润洗滴定管2-3次,取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处,把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液,调节液面至“0”或“0”刻度以下,记下读数,为3.10mL,取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液,把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。所以答案为D C E A;(2)中,B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差;(3)中,若先用待测溶液润洗锥形瓶,则会使测定结果偏大;(4)中,到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色;(5)中,终点读数为21.10,注意小数点的精确位数;(6)中,根据cv=c1v1
可以得到,0.1000×(21.10-3.10)=20c1,解得c1为0.09000mol·L-1。
点评:该题考查了如何配置溶液以及酸碱滴定的相关知识,难度不大,解答该题要注意仪器的读数所精确的位数。

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目

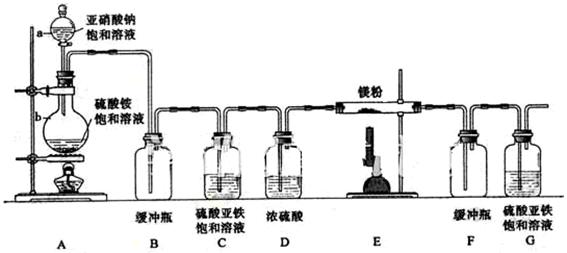
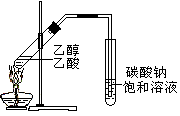
 、
、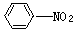 、 己炔、 乙酸四种物质,正确的是
、 己炔、 乙酸四种物质,正确的是