题目内容
【题目】下列说法,可以表明反应N2 + 3H2![]() 2NH3已达到平衡的标志是
2NH3已达到平衡的标志是
A. 1molN≡N键断裂的同时,有6molN-H键形成
B. 1molN≡N键断裂的同时,有3molH-H键断裂
C. 1molN≡N键断裂的同时,有3molH-H键形成
D. 1molN≡N键断裂的同时,有2molN-H键断裂
【答案】C
【解析】
在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此判断。
A. 1molN≡N键断裂的同时,有6molN-H键形成均表示正反应速率,不能说明正逆反应速率相等,A错误;
B. 1molN≡N键断裂的同时,有3molH-H键断裂均表示正反应速率,不能说明正逆反应速率相等,B错误;
C. 1molN≡N键断裂的同时,有3molH-H键形成,反应速率的方向相反,且满足速率之比是相应的化学计量数之比,可以说明反应达到平衡状态,C正确;
D. 1molN≡N键断裂的同时,有2molN-H键断裂,反应速率的方向相反,但不满足速率之比是相应的化学计量数之比,不能说明反应达到平衡状态,D错误。
答案选C。

【题目】利用硫铁矿烧渣(主要成分为Fe2O3,还含有少量Al2O3、 MgO、SiO2等杂质)制备铁红工艺流程如下:

回答下列问题:
(1)还原焙烧后,Fe元素的化合价为__________。
(2)“酸浸”实验中,需加入絮凝剂沉淀杂质。絮凝剂用量和过滤时间对铁红成份的影响如下表所示。由表可知,所采用的最佳实验条件为__________。
絮凝剂用量/×10-6t | 过滤时间min | Fe2O3含量% | SiO2含量% |
40 | 5 | 96.5 | 0.12 |
50 | 10 | 97.9 | 0.10 |
60 | 20 | 98.3 | 0.07 |
100 | 40 | 99.4 | 0.01 |
150 | 150 | 99.5 | 0.008 |
(3)若“合成”中c(Mg2+)=0.01mol/L,加入NH4HCO3(设溶液体积增加1倍),当Fe2+恰好沉淀完全时,溶液中c(Fe2+)=1.0×10-5mol/L,此时是否有MgCO3沉淀生成?_______(列式计算)。FeCO3、MgCO3的Ksp分别为3.2×10-11、3.0×10-8。
(4)“合成”过程中发生反应的离子方程式为_____________.
(5)“合成”过程中温度对亚铁离子转化率的影响如下图,分析选择反应温度为40℃的原因是________。

(6)“煅烧”中由FeCO3制备Fe 2O3的化学方程式为___________。
(7)本流程中,铝元素是以________(填化学式)span>形式被除去的。
【题目】完成如下有关硫的化合物的问题。
(1)硫化物与充足的氧气反应会转化为SO2,写出硫化铝在充足的空气中灼烧的反应方程式________________________________________________。
(2)SO2作为一种化学性质活泼的物质,它能发生多种反应,请按照下表提示,从不同角度梳理SO2的化学性质,将化学方程式填在下表中。
SO2性质梳理 | 化学方程式 | |
物质 类别 | 酸性 氧化物 | SO2+H2O |
SO2+CaO=CaSO3 | ||
①______ | ||
S元素 价态 | S为 +4价 | ②______ |
SO2 +2H2S=3S+2H2O | ||
(3)在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成。
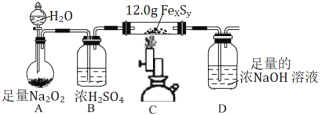
实验步骤:
步骤Ⅰ 如图连接装置,检查装置气密性,装入药品;
步骤Ⅱ 打开A的滴液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间;
步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
步骤Ⅴ 取25.00 mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66 g。
请回答:
①经测定,步骤Ⅳ所得溶液呈强碱性,其中含有的溶质除NaOH外,还可能有______(填化学式)。
②步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为__________。
③在C、D装置之间不需要防倒吸装置的理由是_____________________________。
④步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有________________。
⑤FexSy的化学式为______________。





