题目内容
【题目】海带中含有碘元素。某实验小组设计了如下实验流程,通过实验证明海带中存在碘元素,并从海带中提取出碘单质。

根据实验流程回答下列各题:
(1)步骤①中灼烧所用到硅酸盐材质的仪器,除酒精灯外还有______。
(2)步骤③的操作名称为______。
(3)经过步骤③以后,所得滤液中主要含有可溶性的无机盐:氯化钠、硫酸钠、碘化钠等。为了将I-变为碘单质,可加入经硫酸酸化的双氧水氧化,写出该反应的离子方程式______。检验步骤④是否成功的方法是______。
(4)步骤⑤操作名称是______。
(5)为了进一步制得纯净的碘单质,可以通过步骤⑥实现,实验装置如下图所示。
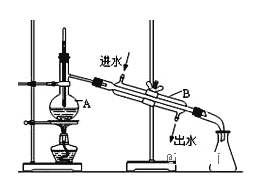
已知实验中得到的粗碘为碘的CCl4溶液,CCl4的沸点76.8℃、I2的沸点184.4℃。
①指出图中错误的地方并改正______。
②锥形瓶中先收集到的物质是______。
【答案】坩埚、泥三角过滤2I-+2H++H2O2=2H2O+I2取少量溶液加入淀粉,看溶液是否变蓝萃取和分液蒸馏烧瓶加热时应垫石棉网,温度计水银球应该在支管口附近,冷凝水应该下进上出CCl4
【解析】
(1)灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,所以还缺少硅酸盐材质的仪器为坩埚、泥三角;
(2)将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法,即步骤③的操作名称为过滤;
(3)含碘离子溶液中加入氧化剂双氧水是为了将碘离子氧化成单质碘,离子方程式为2I-+2H++H2O2=2H2O+I2;碘遇淀粉显蓝色,所以检验步骤④是否成功的方法是取少量溶液加入淀粉,看溶液是否变蓝,如果变蓝,说明还有单质碘;
(4)利用碘易溶于有机溶剂的性质来进行提取,所以步骤⑤操作名称是萃取和分液;
(5)①根据装置图可知蒸馏烧瓶加热时应垫石棉网,温度计水银球应位于蒸馏烧瓶支管口处,冷凝管冷凝水应该是下进上出;
②由于四氯化碳的沸点低于碘,所以锥形瓶中先收集到的物质是CCl4。

 应用题作业本系列答案
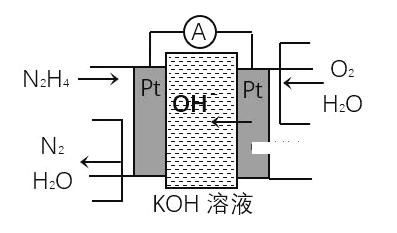
应用题作业本系列答案【题目】(1)肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂。肼燃料电池原理如图所示,通入氧气的电极上发生的电极反应式为____________________。
(2)在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①到达平衡时NO的转化率为_________。
②用O2表示从0~2 s内该反应的平均速率v=____________________。
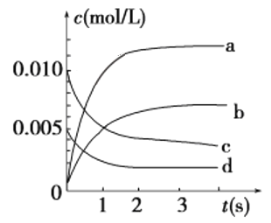
③如下图所示,表示NO2变化曲线的是________。
④能说明该反应已达到平衡状态的是________(填序号)。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内的密度保持不变