题目内容
【题目】完成如下有关硫的化合物的问题。
(1)硫化物与充足的氧气反应会转化为SO2,写出硫化铝在充足的空气中灼烧的反应方程式________________________________________________。
(2)SO2作为一种化学性质活泼的物质,它能发生多种反应,请按照下表提示,从不同角度梳理SO2的化学性质,将化学方程式填在下表中。
SO2性质梳理 | 化学方程式 | |
物质 类别 | 酸性 氧化物 | SO2+H2O |
SO2+CaO=CaSO3 | ||
①______ | ||
S元素 价态 | S为 +4价 | ②______ |
SO2 +2H2S=3S+2H2O | ||
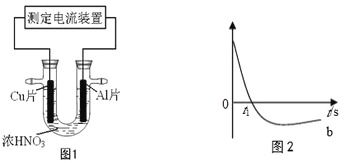
(3)在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成。

实验步骤:
步骤Ⅰ 如图连接装置,检查装置气密性,装入药品;
步骤Ⅱ 打开A的滴液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间;
步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
步骤Ⅴ 取25.00 mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66 g。
请回答:
①经测定,步骤Ⅳ所得溶液呈强碱性,其中含有的溶质除NaOH外,还可能有______(填化学式)。
②步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为__________。
③在C、D装置之间不需要防倒吸装置的理由是_____________________________。
④步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有________________。
⑤FexSy的化学式为______________。
【答案】2Al2S3+9O2 ![]() 2Al2O3+6SO2SO2+2NaOH=Na2SO3+H2OSO2+H2O2=H2SO4Na2SO3与Na2SO4继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收SO2中含不溶于NaOH溶液的O2250mL容量瓶、胶头滴管FeS2
2Al2O3+6SO2SO2+2NaOH=Na2SO3+H2OSO2+H2O2=H2SO4Na2SO3与Na2SO4继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收SO2中含不溶于NaOH溶液的O2250mL容量瓶、胶头滴管FeS2
【解析】
(1)硫化物与充足的氧气反应会转化为SO2,因此硫化铝在充足的空气中灼烧生成二氧化硫和氧化铝,反应的反应方程式为2Al2S3+9O2 ![]() 2Al2O3+6SO2。
2Al2O3+6SO2。
(2)二氧化硫作为一种酸性氧化物,能与碱反应生成盐和水,反应的方程式为SO2+2NaOH=Na2SO3+H2O;+4价的硫能被氧化为+6价,例如SO2+H2O2=H2SO4;
(3)①反应生成的二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,亚硫酸钠不稳定易被氧化为硫酸钠,则步骤Ⅳ所得溶液的溶质除NaOH外,还可能有Na2SO3与Na2SO4;
②过氧化钠与水反应生成氧气,则步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间的目的为继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被吸收。
③由于SO2中含不溶于NaOH溶液的O2,因此在C、D装置之间不需要防倒吸装置;
④步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有250mL容量瓶、胶头滴管;
⑤4.66g沉淀是硫酸钡,物质的量是0.02mol,根据硫原子守恒可知S元素的物质的量是0.02mol,质量是0.02mol×32g/mol=0.64g;所以12g硫化物中Fe的质量是12g-0.64g×250mL/25mL=5.6g,物质的量是0.1mol,因此x:y=0.1:0.2=1:2,所以FexSy的化学式为FeS2。

 中考解读考点精练系列答案
中考解读考点精练系列答案