题目内容
研究表明,SO2水溶液中存在着如下所示多个平衡,向该溶液中( )
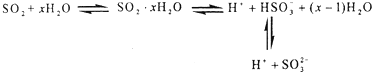
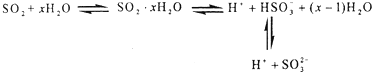
| A、滴加石蕊试液,先变红后褪色 |
| B、滴加品红溶液,先褪色后变红 |
| C、通入硫化氢气体,溶液pH先升高后降低 |
| D、加入足量氯化钡溶液,有白色沉淀生成 |
考点:二氧化硫的化学性质
专题:元素及其化合物
分析:A.二氧化硫为酸性氧化物;
B.二氧化硫具有漂白性;
C.亚硫酸和硫化氢发生氧化还原反应;
D.加入足量氯化钡溶液,不反应.
B.二氧化硫具有漂白性;
C.亚硫酸和硫化氢发生氧化还原反应;
D.加入足量氯化钡溶液,不反应.
解答:
解:A.二氧化硫为酸性氧化物,则滴加石蕊试液,溶液变红,而不褪色,故A错误;
B.二氧化硫具有漂白性,则滴加品红溶液,溶液褪色,若加热恢复红色,故B错误;
C.亚硫酸和硫化氢发生氧化还原反应为H2SO3+2H2S=3S↓+3H2O,溶液的pH先升高,随硫化氢的通入,过量后溶液又显酸性,则溶液的pH又降低,故C正确;
D.盐酸酸性大于亚硫酸,氯化钡和亚硫酸不反应,不会产生亚硫酸钡沉淀,故D错误;
故选C.
B.二氧化硫具有漂白性,则滴加品红溶液,溶液褪色,若加热恢复红色,故B错误;
C.亚硫酸和硫化氢发生氧化还原反应为H2SO3+2H2S=3S↓+3H2O,溶液的pH先升高,随硫化氢的通入,过量后溶液又显酸性,则溶液的pH又降低,故C正确;
D.盐酸酸性大于亚硫酸,氯化钡和亚硫酸不反应,不会产生亚硫酸钡沉淀,故D错误;
故选C.
点评:本题考查二氧化硫的性质,为高频考点,把握二氧化硫为酸性氧化物,具有还原性、漂白性为解答的关键,注意反应与现象的分析,题目难度不大.

练习册系列答案
相关题目
按微粒的半径从大到小的顺序排列的是( )
| A、Mg、Al、Na |
| B、Li、Na、K |
| C、Cl、S、P |
| D、N、O、F |
微粒甲与微粒乙在溶液中的转化关系如图所示: ,微粒甲不可能是( )
,微粒甲不可能是( )
 ,微粒甲不可能是( )
,微粒甲不可能是( )| A、CO2 |
| B、NH4+ |
| C、Al3+ |
| D、SiO2 |
下列有关说法错误的是( )
| A、医药中常用酒精消毒,是因为酒精能使细菌蛋白变性 |
| B、聚酯纤维、光导纤维都属于有机高分子材料 |
| C、对废旧电池回收处理是为了防止重金属污染水源和土壤 |
| D、绿色化学的核心是从源头上减少和消除化工生产对环境的污染 |
下列判断错误的是( )
| A、沸点:NH3>AsH3>PH3 |
| B、熔点:SiO2>CO2>CS2 |
| C、酸性:H2SO4>H3PO4>H2CO3 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
科学家及一些实业家的贡献对科学的发展起着积极地推动作用.下列对有关科学家及其发明创造的叙述,错误的是( )
| A、拉瓦锡证明了化学反应中的质量守恒,建立了燃烧的新理论 |
| B、舍勒发现了氯气,凯库勒提出了苯的结构式 |
| C、侯德榜发明了“候氏制碱”法,吴蕴初开创了中国的氯碱工业 |
| D、道尔顿、汤姆孙、卢瑟福和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
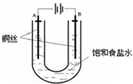 已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )
已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )| A、B极发生的电极反应为2H++2e-=H2↑ |
| B、实验开始时,A极附近出现白色浑浊 |
| C、电解时,Na+移向A极 |
| D、一段时间后,U形管底部形成橙黄色沉淀 |
25℃时,pH值都等于11的NaOH溶液和Na2CO3溶液中,由水电离出的OH-浓度( )
| A、相等,均为10-3mol?L-1 |
| B、相等,均为10-11mol?L-1 |
| C、NaOH溶液中为10-3mol?L-1 |
| D、Na2CO3溶液中为10-3mol?L-1 |
铅蓄电池是一种用途极广的二次电池,其电池反应为:下列说法不正确的是( )
Pb+PbO2+2H2SO4
2PbSO4(s)+2H2O.
Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
| A、放电时,负极质量增加 |
| B、充电时,应将外接直流电源的正极与蓄电池的铅电极相接 |
| C、放电时,正极反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| D、铅蓄电池做电源电解Na2SO4溶液时,当有1mol O2产生时,消耗4mol H2SO4 |