题目内容
25℃时,pH值都等于11的NaOH溶液和Na2CO3溶液中,由水电离出的OH-浓度( )
| A、相等,均为10-3mol?L-1 |
| B、相等,均为10-11mol?L-1 |
| C、NaOH溶液中为10-3mol?L-1 |
| D、Na2CO3溶液中为10-3mol?L-1 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:氢氧化钠为强碱溶液,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的;碳酸钠溶液中,碳酸根离子水解促进了水的电离,溶液中氢氧根离子为水电离的,据此进行判断.
解答:
解:25℃时,pH值等于11的NaOH溶液中,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的,水电离的氢离子浓度为:1×10-11mol/L;
pH=11的碳酸钠溶液中,碳酸根离子水解促进了水的电离,溶液中氢氧根离子是水电离的,水电离的氢离子浓度为:
mol/L=1×10-3mol/L,
故选D.
pH=11的碳酸钠溶液中,碳酸根离子水解促进了水的电离,溶液中氢氧根离子是水电离的,水电离的氢离子浓度为:
| 1×10-14 |
| 1×10-11 |
故选D.
点评:本题考查水的电离及其影响因素,难度不大.注意明确酸溶液、碱溶液抑制水的电离,能够水解的盐溶液促进水的电离.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列叙述正确的是( )
| A、将NH3通过热的CuO,有红色固体生成 |
| B、将SO2通入过量BaCl2溶液可生成BaSO3沉淀 |
| C、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| D、Li在氧气中燃烧主要生成Li2O2 |
研究表明,SO2水溶液中存在着如下所示多个平衡,向该溶液中( )
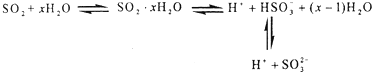
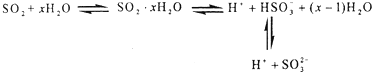
| A、滴加石蕊试液,先变红后褪色 |
| B、滴加品红溶液,先褪色后变红 |
| C、通入硫化氢气体,溶液pH先升高后降低 |
| D、加入足量氯化钡溶液,有白色沉淀生成 |
下列关于SO2性质的分析,正确的是( )
| A、通入BaCl2溶液中,有白色沉淀生成 |
| B、通入FeCl3溶液中,有SO42-生成 |
| C、通入氯水中,有淡黄色沉淀生成 |
| D、通入KI溶液中,有I2生成 |
下列实验不能达到预期目的是( )
| A、用饱和NaHCO3溶液除去CO2中少量的HCl |
| B、用醋和澄清石灰水验证蛋壳中含有碳酸盐 |
| C、在试管中煮沸液体时,加碎石片可防止暴沸 |
| D、用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
已知,25℃时有关弱酸的电离平衡常数如下表:下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7,K2=5.6×l0-11 |
| A、测得1000mL 0.50mol/L盐酸与1000mL 0.55mol/L NaOH溶液混合时放出28.65kJ的热量,则稀醋酸和稀NaOH溶液反应的△H=-57.3kJ?mol-1 | ||
| B、冰醋酸中逐滴加水,溶液的导电性和pH、醋酸的电离程度均先增大后减小 | ||
| C、向NaCN溶液中通入少量CO2:2CN-+CO2+H2O═2HCN+CO32- | ||
D、将0.1mol/L的醋酸溶液加水稀释,则
|
已知二氯化二硫(S2Cl2)的结构式为Cl-S-S-Cl,它易与水反应2S2Cl2+2H2O→4HCl+SO2↑+3S↓.在该反应中( )
| A、S2Cl2既作氧化剂又作还原剂 |
| B、氧化产物与还原产物物质的量比为3:1 |
| C、每生成22.4L SO2转移3mol电子 |
| D、每生成48g硫会断裂6mol共价键 |
下列说法正确的是( )
| A、乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 |
| B、所有烷烃和蛋白质分子中都存在碳碳单键 |
| C、人们通常用聚乙烯、聚氯乙烯塑料来制食品包装袋,它们都是高分子化合物 |
| D、苯和乙烯都能使溴水退色,其褪色原理是相同的 |
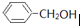 四种有机物
四种有机物