题目内容
按微粒的半径从大到小的顺序排列的是( )
| A、Mg、Al、Na |
| B、Li、Na、K |
| C、Cl、S、P |
| D、N、O、F |
考点:微粒半径大小的比较
专题:元素周期律与元素周期表专题
分析:同周期自左而右原子半径减小,同主族自上而下原子半径增大,据此判断.
解答:
解:A.Na、Mg、Al同周期,自左而右原子半径减小,故原子半径:Na>Mg>Al,故A错误;
B.Li、Na、K同主族,自上而下原子半径增大,故原子半径:Li<Na<K,故B错误;
C.Cl、S、P同周期,自左而右原子半径减小,故原子半径:Cl<S<P,故C错误;
D.N、O、F同周期,自左而右原子半径减小,故原子半径:N>O>F,故D正确,
故选D.
B.Li、Na、K同主族,自上而下原子半径增大,故原子半径:Li<Na<K,故B错误;
C.Cl、S、P同周期,自左而右原子半径减小,故原子半径:Cl<S<P,故C错误;
D.N、O、F同周期,自左而右原子半径减小,故原子半径:N>O>F,故D正确,
故选D.
点评:本题考查原子半径比较,难度不大,注意理解掌握同周期、同主族原子半径递变规律.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组溶液中,离子一定能大量共存的是( )
| A、强碱溶液中:Na+、Mg2+、SO42-、AlO2- |
| B、某无色溶液中:NH4+、Fe3+、MnO4-、NO3- |
| C、含有0.1mol/L Fe3+溶液中:K+、Mg2+、Cl-、SCN- |
| D、与铝反应生成H2的溶液中:Na+、K+、Cl-、SO42- |
从反应结果分析,下列关于“反应先后顺序”的评价中正确的是( )
| A、向物质的量比为1:1的Na2CO3和NaOH混合溶液中通入少量CO2,NaOH先发生反应 |
| B、向体积比为1:1的SO2和CO2混合气体中加入少量氨水,CO2先发生反应 |
| C、向物质的量之比为1:1的FeCl3和CuCl2混合溶液中加入少量Fe粉,Cu2+先被还原 |
| D、向NH4Al(SO4)2溶液中滴加少量NaOH溶液,NH4+先发生反应 |
能以离子键相结合生成AB型(B为阴离子)离子化合物,它们的原子序数分别为( )
| A、11和17 | B、11和16 |
| C、20和9 | D、13和17 |
向两份a mL b mol/L的稀盐酸中分别加入x mL的水和y mL b mol/L Ba(OH)2溶液,此时两溶液的pH恰好相等,则x、y的关系符合(式中a、b均大于零,设两溶液混合时的体积有加和性)( )
| A、y=2ax+b | ||||
B、y=
| ||||
C、
| ||||
D、x=
|
下列叙述正确的是( )
| A、将NH3通过热的CuO,有红色固体生成 |
| B、将SO2通入过量BaCl2溶液可生成BaSO3沉淀 |
| C、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| D、Li在氧气中燃烧主要生成Li2O2 |
研究表明,SO2水溶液中存在着如下所示多个平衡,向该溶液中( )
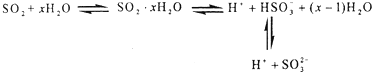
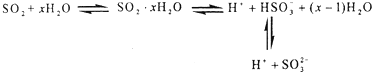
| A、滴加石蕊试液,先变红后褪色 |
| B、滴加品红溶液,先褪色后变红 |
| C、通入硫化氢气体,溶液pH先升高后降低 |
| D、加入足量氯化钡溶液,有白色沉淀生成 |
