题目内容
铅蓄电池是一种用途极广的二次电池,其电池反应为:下列说法不正确的是( )
Pb+PbO2+2H2SO4
2PbSO4(s)+2H2O.
Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
| A、放电时,负极质量增加 |
| B、充电时,应将外接直流电源的正极与蓄电池的铅电极相接 |
| C、放电时,正极反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| D、铅蓄电池做电源电解Na2SO4溶液时,当有1mol O2产生时,消耗4mol H2SO4 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铅蓄电池负极材料为Pb,电极反应为:Pb+SO42--2e-=PbSO4↓,正极材料为PbO2,电极反应为:PbO2+SO42-+4H++2e-=PbSO4↓+2H2O,
电池总反应为Pb+PbO2+2H2SO4
2PbSO4(s)+2H2O,以此解答该题.
电池总反应为Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
解答:
解:A.放电时,负极发生Pb+SO42--2e-=PbSO4↓,负极质量增加,故A正确;
B.充电时,应将外接直流电源的正极与蓄电池的正极相连,即与PbO2电极相连,故B错误;
C.放电时,正极发生还原反应,电极方程式反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,故C正确;
D.当有1mol O2产生时,转移4mol电子,由总方程式Pb+PbO2+2H2SO4
2PbSO4(s)+2H2O可知,消耗4mol硫酸,故D正确.
故选B.
B.充电时,应将外接直流电源的正极与蓄电池的正极相连,即与PbO2电极相连,故B错误;
C.放电时,正极发生还原反应,电极方程式反应为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,故C正确;
D.当有1mol O2产生时,转移4mol电子,由总方程式Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
故选B.
点评:本题考查原电池的工作原理,为高频考点,侧重于学生的分析能力的考查,题目难度中等,本题注意电极反应式的书写,为解答该题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
研究表明,SO2水溶液中存在着如下所示多个平衡,向该溶液中( )
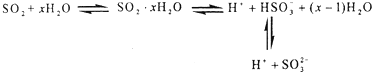
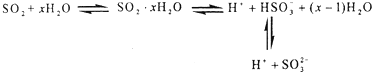
| A、滴加石蕊试液,先变红后褪色 |
| B、滴加品红溶液,先褪色后变红 |
| C、通入硫化氢气体,溶液pH先升高后降低 |
| D、加入足量氯化钡溶液,有白色沉淀生成 |
已知二氯化二硫(S2Cl2)的结构式为Cl-S-S-Cl,它易与水反应2S2Cl2+2H2O→4HCl+SO2↑+3S↓.在该反应中( )
| A、S2Cl2既作氧化剂又作还原剂 |
| B、氧化产物与还原产物物质的量比为3:1 |
| C、每生成22.4L SO2转移3mol电子 |
| D、每生成48g硫会断裂6mol共价键 |
下列说法正确的是( )
| A、乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 |
| B、所有烷烃和蛋白质分子中都存在碳碳单键 |
| C、人们通常用聚乙烯、聚氯乙烯塑料来制食品包装袋,它们都是高分子化合物 |
| D、苯和乙烯都能使溴水退色,其褪色原理是相同的 |
下列说法中正确的是( )
| A、分离Al2O3与Fe2O3混合物可以采取加入过量NaOH溶液充分反应后,过滤、洗涤、干燥 |
| B、用过量氨水除去Fe3+溶液中的少量Al3+ |
| C、将Mg(OH)2放入表面皿中,加入足量盐酸,加热蒸干得无水MgCl2 |
| D、Al(OH)3中混有Mg(OH)2;加入足量烧碱溶液,充分反应过滤,向滤液中通入足量二氧化碳后过滤、洗涤、干燥 |
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理.下列叙述正确的是( )
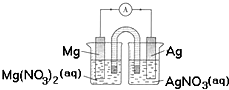

| A、银片为负极,发生的反应为:Ag++e-=Ag |
| B、进行实验时,琼脂中K+移向Mg(NO3)2溶液 |
| C、用稀硫酸代替AgNO3溶液,可形成原电池 |
| D、取出盐桥,电流表依然有偏转 |
下列方法能用于鉴别二甲醚(CH3OCH3)和乙醇的是( )
| A、李比希燃烧法 |
| B、铜丝燃烧法 |
| C、红外光谱法 |
| D、元素分析仪 |
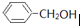 四种有机物
四种有机物