题目内容
9.下列说法中,正确的是( )| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 燃煤发电是煤的综合利用的重要途径 | |
| C. | 反应物的总能量大于生成物的总能量的化学反应是放热反应 | |
| D. | 化学键的断裂和形成与化学变化中的能量变化无关 |
分析 A.反应是吸热反应还是放热反应与反应的条件无关;
B.气化、液化和干馏是煤综合利用的主要方法;
C.放热反应中反应物总能量高于生成物总能量;
D.断键吸收能量、成键放出能量.
解答 解:A.因反应是吸热反应还是放热反应与反应的条件无关,如铝热反应需要加热才能发生,却为放热反应,故A错误;
B.气化、液化和干馏是煤综合利用的主要方法,燃煤发电不是,故B错误;
C.反应中反应物总能量高于生成物总能量,说明该反应是一个放热反应,故C错误;
D.化学反应中能量变化的主要原因是化学键的断裂和形成,故D正确.
故选D.
点评 本题主要考查了化学反应中能量变化的原因,需要注意的是反应是吸热反应还是放热反应与反应的条件无关,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
20.同温同浓度的条件下,NaHCO3和NaHSO4溶液中水的电离程度前者与后者之间的关系是( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能确定 |
17.将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中充分反应后,放出氢气最多的是( )
| A. | 3mol/LHCl | B. | 4mol/LHNO3 | C. | 8mol/LNaOH | D. | 18mol/LH2SO4 |
4.燃料电池是目前正在探索的一种新型电池,现在已经使用的氢氧燃料电池的基本反应是:x 极:O2(g)+2H2O(l)+4e-═4OH- y极:2H2(g)+4OH--4e-═4H2O(l) 判断下列说法中正确的是( )
| A. | x极为电池的负极 | B. | x极附近溶液的pH值减小 | ||
| C. | y极发生氧化反应 | D. | 电流由y极流向x极 |
14.下列关于常见有机物的说法不正确的是( )
| A. | 乙烯和甲烷可用酸性高锰酸钾溶液鉴别 | |
| B. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| C. | 2-戊烯存在顺反异构现象 | |
| D. | 乙烯和苯都能与酸性高锰酸钾溶液、溴水反应 |
1. 下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
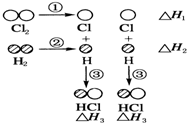
H2和Cl2反应生成HCl过程中的热效应可用如图表示,请回答下列问题:
(1)△H1=+243kJ•mol-1,△H2=+436kJ•mol-1,△H3=-431kJ•mol-1.
(2)该反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ•mol-1.
 下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):
下表中的数据表示破坏1mol物质中的化学键需消耗的能量(即键能):| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能/kJ•mol-1 | 436 | 243 | 431 |
(1)△H1=+243kJ•mol-1,△H2=+436kJ•mol-1,△H3=-431kJ•mol-1.
(2)该反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-183 kJ•mol-1.
16.与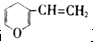 互为同分异构体,其中遇氯化铁溶液显紫色和不显紫色的芳香族化合物分别有( )
互为同分异构体,其中遇氯化铁溶液显紫色和不显紫色的芳香族化合物分别有( )
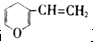 互为同分异构体,其中遇氯化铁溶液显紫色和不显紫色的芳香族化合物分别有( )
互为同分异构体,其中遇氯化铁溶液显紫色和不显紫色的芳香族化合物分别有( )| A. | 3种和2种 | B. | 2种和2种 | C. | 2种和1种 | D. | 3种和1种 |
 X、Y、Z、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于同一周期,其中基态Y原子的2p轨道处于半充满状态,Y和Z的单质可以通过分离液态空气的方法大量制得,且XZ2与Y2Z互为等电子体.含U的化合物的焰色为紫色.试回答下列问题:
X、Y、Z、U为原子序数依次增大的前四周期元素,X、Y、Z三种元素位于同一周期,其中基态Y原子的2p轨道处于半充满状态,Y和Z的单质可以通过分离液态空气的方法大量制得,且XZ2与Y2Z互为等电子体.含U的化合物的焰色为紫色.试回答下列问题: 2SO2(g)+O2(g);△H =+196.6 kJ/mol
2SO2(g)+O2(g);△H =+196.6 kJ/mol