题目内容
5.NH4+、NO3-、HSO4-、HCO3-、CO32-、HCl等微粒中,在水溶液里能电离而不能水解的有HCl,HSO4-;能水解而不能电离的有NH4+,CO32-;既能水解又能电离的有HCO3-;既不能水解又不能电离的有NO3-.写出其中既能水解又能电离的微粒的电离方程式及水解方程式HCO3-═H++CO32-,HCO3-+H2O═H2CO3+OH-.分析 给出的微粒中,酸式酸根离子、酸能发生电离,强酸或强碱对应的离子不能水解;弱酸、弱碱的离子能水解,以此来解答.
解答 解:HSO4-、HCl在水溶液里能电离而不能水解;
NH4+、CO32-能水解而不能电离;
HCO3-既能水解又能电离,其电离方程式及水解方程式分别为HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-,
既不能水解又不能电离的是NO3-,
故答案为:HSO4-,HCl;NH4+,CO32-;HCO3-;NO3-;HCO3-═H++CO32-,HCO3-+H2O═H2CO3+OH-.
点评 本题考查电离与水解,注意电离与水解的规律及弱电解质的电离、盐类水解均为可逆反应,注重基础知识的考查,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
18.同体积的1mol/L的HCl、H2SO4、CH3COOH分别加入过量的Mg.下列叙述中正确的是( )
| A. | HCl、H2SO4中放出H2的速率相同 | |
| B. | CH3COOH中放出H2的速率最快 | |
| C. | H2SO4中放出H2的速率最快,CH3COOH中放出H2的速率最慢 | |
| D. | H2SO4中放出H2的量最多,其余的相等 |
16.下列有机物分子中,所有的原子不可能处于同一平面的是( )
| A. | CH2=CH-CI | B. | CH2=CH-CH=CH2 | C. | CH3-CH=CH2 | D. | 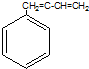 |
20.同温同浓度的条件下,NaHCO3和NaHSO4溶液中水的电离程度前者与后者之间的关系是( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能确定 |
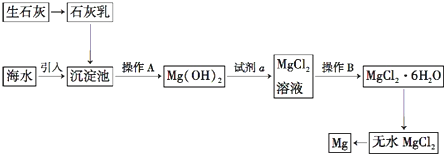
10. 如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
 如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| 甲 | 乙 | 丙 | 丁 | |
| ① | Cu | CuO | CuCl2 | Cu(NO3)2 |
| ② | Na2CO3 | NaOH | NaHCO3 | CO2 |
| ③ | (NH4)2SO3 | CaSO3 | SO2 | NH4HSO3 |
| ④ | Al(OH)3 | Al2O3 | NaAlO2 | AlCl3 |
| A. | ①②③④ | B. | 仅②③④ | C. | 仅②④ | D. | 仅③④ |
17.将等物质的量的镁和铝相混合,取等质量该混合物四份,分别加到足量的下列溶液中充分反应后,放出氢气最多的是( )
| A. | 3mol/LHCl | B. | 4mol/LHNO3 | C. | 8mol/LNaOH | D. | 18mol/LH2SO4 |
14.下列关于常见有机物的说法不正确的是( )
| A. | 乙烯和甲烷可用酸性高锰酸钾溶液鉴别 | |
| B. | 乙酸和油脂都能与氢氧化钠溶液反应 | |
| C. | 2-戊烯存在顺反异构现象 | |
| D. | 乙烯和苯都能与酸性高锰酸钾溶液、溴水反应 |