题目内容
【题目】过氧乙酸(![]() ),是一种高效消毒剂,它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
),是一种高效消毒剂,它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:

①在三颈烧瓶中加入一定量冰醋酸与浓硫酸的混合物,再缓缓加入适量30%的双氧水;
②不断搅拌并控制装置B中混合液的温度为20~30℃至反应结束;
③接入仪器C和抽气泵,在锥形瓶中收集得到产品。
回答下列问题:
(1)仪器C的名称是____,仪器C中冷水流入口是____(填“a”或“b”)。
(2)为更好地控制反应温度,应采用的加热方法是_____。
(3)生成过氧乙酸的化学方程式为____。
(4)实验测得产物过氧乙酸的百分含量随反应物比例和反应时间的变化数据如下表。由表中数据可知,反应物最佳比例(CH3COOH/H2O2)是_____,最佳反应时间约_____。
反应物比例CH3COOH/H2O2 | 反应时间 | ||||
0.5h | 1h | 3h | 5h | 7h | |
2:1 | 7.38% | 8.46% | 9.42% | 11.26% | 13.48% |
1:1 | 0.56% | 12.92% | 13.54% | 20.72% | 20.80% |
1:2 | 6.14% | 7.10% | 7.96% | 10.38% | 12.36% |
(5)产品中过氧乙酸浓度的测定:取2.00mL过氧乙酸产品试样,加水稀释成100mL;从中取出5.00mL,逐滴滴加酸性KMnO4溶液至溶液恰好呈粉红色,以除去残余的H2O2;再加入稍过量的KI溶液,发生反应CH3COOOH+2I-+2H+=I2+CH3COOH+H2O;反应完全后,滴入几滴淀粉溶液,用0.1000mol·L-1的Na2S2O3标准液滴定至终点(反应式为2S2O32-+I2=S4O62-+2I-
【答案】直形冷凝管 a 水浴加热 CH3COOH+H2O2![]() CH3COOOH+H2O 1:1 5h 7.15
CH3COOOH+H2O 1:1 5h 7.15
【解析】
(1)由仪器结构,可知C为直形冷凝管,采取逆流原理通入冷凝水;
(2)控制B中混合液的温度为20~30℃,应采取水浴加热;
(3)根据元素守恒和物质的结构特点写出方程式;
(4)生成的过氧乙酸含量越高越好,结合表格中数据选择;
(5)根据关系式:CH3COOOH~I2~2Na2S2O3,计算稀释后的5mL溶液中过氧乙酸的物质的量,进而计算原来的2mL溶液中过氧乙酸的物质的量,在根据物质的量浓度定义式计算。
(1)由仪器结构,可知C为直形冷凝管,采取逆流原理通入冷凝,使冷凝管充满冷凝水,充分进行冷凝,即由a口进水、b口出水,
故答案为:直形冷凝管;a;
(2)控制B中混合液的温度为20~30℃,应采取水浴加热,受热均匀,便于控制温度,
故答案为:水浴加热;
(3)乙酸与过氧化氢在浓硫酸、20~30℃条件下反应生成 CH3COOOH,乙酸羧基中H原子被过氧化氢的-OH替代,同时生成H2O,生成过氧乙酸的化学方程式为为:CH3COOH+H2O2 ![]() CH3COOOH+H2O;
CH3COOOH+H2O;
故答案为:CH3COOH+H2O2 ![]() CH3COOOH+H2O;
CH3COOOH+H2O;
(4)由表中数据可知,反应物比例(CH3COOH/H2O2)是1:1时反应一段时间后过氧乙酸含量较高,且反应时间5小时后增长不再明显,故答案为:1:1;5h;
(5)根据关系式:CH3COOOH~I2~2Na2S2O3,可知稀释后的5mL溶液中过氧乙酸的物质的量=![]() ×0.0143L×0.1000mol/L,原来的2mL溶液中过氧乙酸的物质的量=
×0.0143L×0.1000mol/L,原来的2mL溶液中过氧乙酸的物质的量=![]() ×0.0143L×0.1000mol/Lmol×
×0.0143L×0.1000mol/Lmol×![]() =0.0143mol,故该样品中过氧乙酸的物质的量浓度是
=0.0143mol,故该样品中过氧乙酸的物质的量浓度是![]() =7.15mol/L,故答案为:7.15。
=7.15mol/L,故答案为:7.15。

【题目】甲、乙同学用0.10mol/L H2C2O4草酸溶液、0.01mol/L KMnO4溶液、0.01mol/L H2SO4溶液、一定量的蒸馏水等试剂,进行探究实验,通过测定溶液褪色所需时间来探究浓度、温度对反应速率的影响。
(1)已知酸性KMnO4与H2C2O4反应后Mn元素以Mn2+形式存在溶液中,C元素转化为CO2气体逸出,请写出该反应的化学方程式____________。
(2)为探究反应物浓度、温度对化学反应速率的影响。甲同学设计的实验方案如下表:
实验序号 | 温度/℃ | 体积V/ mL | |||
H2C2O4溶液 | 水 | KMnO4溶液 | H2SO4溶液 | ||
1 | 25 | 10.0 | 0.0 | 4.0 | 2.0 |
2 | 25 | 8.0 | a | 4.0 | 2.0 |
3 | 50 | b | 0.0 | 4.0 | 2.0 |
①若以实验1为对照组,为了达到实验探究目的则a=____________,b=____________。
②若实验1测得溶液褪色所需时间为5s,则用高锰酸钾表示的反应速率为______________________。
(3)乙同学部分实验设计方案如下表:
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
mol/L | mL | mol/L | mL | ||
① | 0.10 | 2.0 | 0.01 | 4.0 | 25 |
② | 0.10 | 2.0 | 0.02 | 4.0 | 25 |
…… | |||||
该同学想通过实验①和②探究反应物浓度对化学反应速率的影响,请你对该方案的合理性进行评价,并说明理由__________________________。
【题目】对甲烷和CO2的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合CO2重整反应有:
反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g) △H=-71.4kJmol-1
2CO(g)+4H2(g) △H=-71.4kJmol-1
反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=+247.0kJmol-1
2CO(g)+2H2(g) △H=+247.0kJmol-1
(1)写出表示CO燃烧热的热化学方程式:_____。
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g)(不发生其它反应),CO2的平衡转化率如下表所示:
起始物质的量(n)/mol | CO2的平衡转化率 | ||||
CH4 | CO2 | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列能说明反应达到平衡状态是_____。
A.v正(CH4)=2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为tmin,则tmin内该反应的平均反应速率为:v(H2)=____(用含t的表达式表示)。
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ___n(CO)Ⅱ(填“>”、“=”或“<”)。
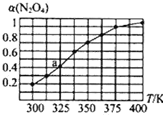
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g)
2CO(g)+4H2(g)
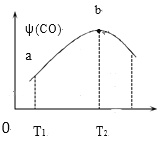
①T2℃时,CO体积分数最大的原因是____。
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP=___(用平衡分压强代替平衡浓度计算,分压=总压×物质的量分数)。
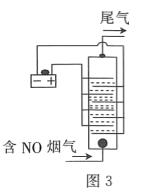
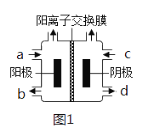
(4)2016年我国科研人员根据反应Na+CO2→Na2CO3+C(未配平)研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:___。
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:___。