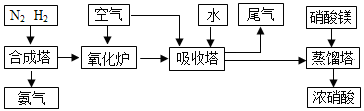
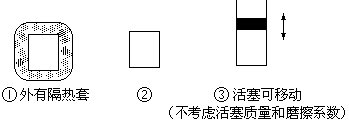
题目内容
将mg的铜放入足量的稀硝酸中充分反应后,生成nL(标准状况)一氧化氮,被还原的硝酸为( )
①
g;②
g;③
mol;④42mmol.
①
| 63n |
| 22.4 |
| n |
| 22.4 |
| m |
| 96 |
| A.①④ | B.①③ | C.②④ | D.②③ |
铜和稀硝酸的离子反应方程式为:3Cu+8H++2NO3-(稀)=3Cu 2++2NO↑+4H2O,根据铜和被还原硝酸之间的关系式知,被还原硝酸的物质的量=
×2=
mol;
硝酸根离子被还原生成一氧化氮,根据氮原子守恒得被还原硝酸的质量=
×63g/mol=
mol×63g/mol=
g,
通过以上分析知,①③正确,
故选B.
| ||
| 3 |
| m |
| 96 |
硝酸根离子被还原生成一氧化氮,根据氮原子守恒得被还原硝酸的质量=
| nL |
| 22.4L/mol |
| n |
| 22.4 |
| 63n |
| 22.4 |
通过以上分析知,①③正确,
故选B.

练习册系列答案
相关题目