题目内容
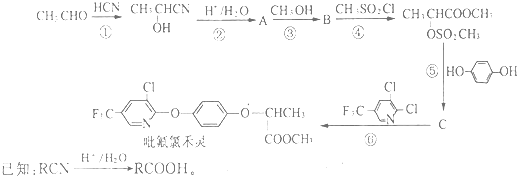
20.经测定有机物A的分子式为C7H6O3,A遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生.化合物A能经下列反应得到W( ).
).
已知:
RCOOH$\stackrel{还原}{→}$RCH2OH
RX$→_{②H_{3}O+}^{①NaCN}$RCOOH
R1COOH+RCH2Cl$\stackrel{一定条件}{→}$R1COOCH2R+HCl
(1)有机物A中含有的官能团的名称羧基、羟基.
(2)下列关于有机物B的说法正确的是bd(填字母代号).
a.能发生水解反应 b.能与浓溴水反应 c.能发生消去反应 d.能与H2发生加成反应
(3)化合物C的结构简式为
 .
.(4)反应D→W的化学方程式为
 .
.(5)反应D+G→H的化学方程式为
 .
.(6)化合物D有多种同分异构体,其中某些同分异构体遇FeCl3溶液显紫色,能发生水解反应,且苯环上的一氯取代产物只有2种,写出这些同分异构体的结构简式
 、
、 、
、 .
.
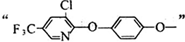
分析 由W的结构,逆推可知D为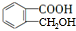 ,由转化关系及反应信息可知,C为
,由转化关系及反应信息可知,C为 .有机物A遇FeCl3水溶液显紫色,说明含有酚羟基,与NaHCO3溶液反应有CO2产生,说明含有羧基,有机物A的分子式为C7H6O3,可知分子中含有1个酚羟基-OH、1个羧基-COOH,A还原得到N,B与HBr反应得到C,结合C的结构可知A为
.有机物A遇FeCl3水溶液显紫色,说明含有酚羟基,与NaHCO3溶液反应有CO2产生,说明含有羧基,有机物A的分子式为C7H6O3,可知分子中含有1个酚羟基-OH、1个羧基-COOH,A还原得到N,B与HBr反应得到C,结合C的结构可知A为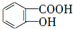 ,则B为
,则B为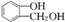 .F与氯气在光照条件下发生取代反应生成G,由G的分子式可知F分子式为C7H8,可推知G为
.F与氯气在光照条件下发生取代反应生成G,由G的分子式可知F分子式为C7H8,可推知G为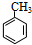 ,E为
,E为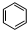 ,F为
,F为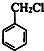 ,F与D发生取代反应生成H为
,F与D发生取代反应生成H为 ,据此解答.
,据此解答.
解答 解:由W的结构,逆推可知D为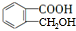 ,由转化关系及反应信息可知,C为
,由转化关系及反应信息可知,C为 .有机物A遇FeCl3水溶液显紫色,说明含有酚羟基,与NaHCO3溶液反应有CO2产生,说明含有羧基,有机物A的分子式为C7H6O3,可知分子中含有1个酚羟基-OH、1个羧基-COOH,A还原得到N,B与HBr反应得到C,结合C的结构可知A为
.有机物A遇FeCl3水溶液显紫色,说明含有酚羟基,与NaHCO3溶液反应有CO2产生,说明含有羧基,有机物A的分子式为C7H6O3,可知分子中含有1个酚羟基-OH、1个羧基-COOH,A还原得到N,B与HBr反应得到C,结合C的结构可知A为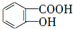 ,则B为
,则B为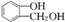 .F与氯气在光照条件下发生取代反应生成G,由G的分子式可知F分子式为C7H8,可推知G为
.F与氯气在光照条件下发生取代反应生成G,由G的分子式可知F分子式为C7H8,可推知G为 ,E为
,E为 ,F为
,F为 ,F与D发生取代反应生成H为
,F与D发生取代反应生成H为 .
.
(1)由上述分析可知,A为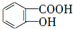 ,含有的官能团的名称:羧基、羟基,故答案为:羧基、羟基;
,含有的官能团的名称:羧基、羟基,故答案为:羧基、羟基;
(2)B为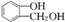 ,含有酚羟基,能与浓溴水反应,含有苯环,能与氢气发生加成反应,不能发生水解反应、消去反应,故选:bd;
,含有酚羟基,能与浓溴水反应,含有苯环,能与氢气发生加成反应,不能发生水解反应、消去反应,故选:bd;
(3)由上述分析可知,化合物C的结构简式为 ,故答案为:
,故答案为: ;
;
(4)反应D→W的化学方程式为: ,
,
故答案为: ;
;
(5)反应D+G→H的化学方程式为: ,
,
故答案为: ;
;
(6)化合物D(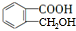 )有多种同分异构体,其中某些同分异构体遇FeCl3溶液显紫色,含有酚羟基,能发生水解反应,含有酯基,且苯环上的一氯取代产物只有2种,应含有2个不同的取代基且处于对位,这些同分异构体的结构简式为:
)有多种同分异构体,其中某些同分异构体遇FeCl3溶液显紫色,含有酚羟基,能发生水解反应,含有酯基,且苯环上的一氯取代产物只有2种,应含有2个不同的取代基且处于对位,这些同分异构体的结构简式为: 、
、 、
、 ,
,
故答案为: 、
、 、
、 .
.
点评 本题考查有机物的推断,注意利用W的结构简式及给予的反应信息、反应条件采取逆推法进行推断,注意理解掌握官能团的引入和消去,是对学生思维能力的考查,难度中等.

| A. | 3:2 | B. | 4:l3 | C. | 3:4 | D. | 3:5 |
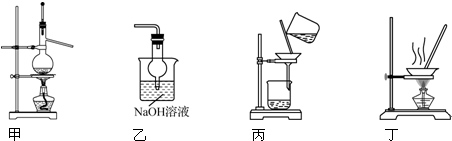
| A. | 用装置甲以乙醇和浓硫酸为原料制乙烯 | |
| B. | 用装置乙吸收某些实验尾气中的二氧化硫 | |
| C. | 用装置丙分离Cl2与KI溶液反应生成的碘 | |
| D. | 用装置丁蒸干NH4Cl饱和溶液获取NH4Cl晶体 |
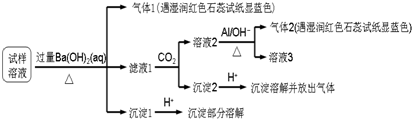
已知:3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 试样中可能含有Al3+ | |
| C. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| D. | 试样中不可能存在Na+、Cl- |
| 序号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | NaOH | CH3COOH | HCl |
| 浓度c/mol•L-1 | 0.01 | 0.01 | 0.01 | 0.01 |
| A. | 由水电离出的c(H+):①=②=③=④ | |
| B. | 溶液的pH:②>①>④>③ | |
| C. | ②、③混合呈中性,所需溶液的体积:③>② | |
| D. | ①、④等体积混合,所得溶液中离子的浓度:c(NH4+)=c(Cl-)>c(H+)=c(OH-) |
| A. | SO3、NO3-、BF3都是平面三角型 | B. | P4、CS2、PH3都是非极性分子 | ||
| C. | 金刚石、石墨、SiC都是原子晶体 | D. | 第一电离能:N>O>C |

 ;
;


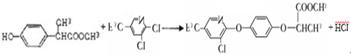
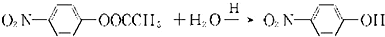 +CH3COOH.
+CH3COOH.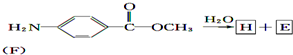
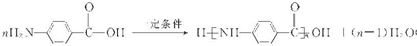 .
.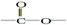 结构.
结构. .
.