题目内容
2.将铜片放入0.1mol/LFeCl3溶液中,反应一定时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为( )| A. | 3:2 | B. | 4:l3 | C. | 3:4 | D. | 3:5 |
分析 反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,根据反应的离子方程式计算.
解答 解:设有生成xmolFe2+,
2Fe3++Cu=2Fe2++Cu2+
2 2 1
x x $\frac{1}{2}$x
反应后c (Fe3+):c(Fe2+)=2:3,
则n(Fe3+)=$\frac{2}{3}$n(Fe2+)=$\frac{2x}{3}$mol,
由方程式可知:生成的Cu2+的物质的量为$\frac{1}{2}$x,
所以反应后的溶液中:n(Cu2+):n(Fe3+)=$\frac{1}{2}$xmol:$\frac{2}{3}$xmol=3:4,
故选C.
点评 本题既考查了化学方程式的有关计算,同时又考查了Fe3+的氧化性,解题的关键是正确书写出化学反应方式,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列说法正确的是( )
| A. | 按系统命名法,化合物(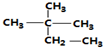 )的名称为2-甲基-2-乙基丙烷 )的名称为2-甲基-2-乙基丙烷 | |
| B. | 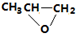 和CO2转化为 和CO2转化为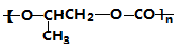 的反应符合绿色化学的原则 的反应符合绿色化学的原则 | |
| C. | 用新制氢氧化铜悬浊液无法检验失去标签的乙醇、乙醛、乙酸三瓶无色溶液 | |
| D. | 乙醇和乙醚互为同分异构体,沸点乙醇比乙醚高 |
17.也许有人告诉过你:“你长着妈妈的眼睛、爸爸的鼻子”.其实,你的眼睛就是你的眼睛,你的鼻子就是你自己的鼻子,但你身体里的蛋白质、基因确实继承于你的父母.核糖[CH2OH(CHOH)3CHO]和脱氧核糖[CH2OH(CHOH)2CH2CHO]是人类生命活动不可缺少的物质,在一定条件下它们都能发生的反应是( )
①氧化 ②还原 ③酯化 ④水解 ⑤加成 ⑥中和.
①氧化 ②还原 ③酯化 ④水解 ⑤加成 ⑥中和.
| A. | ①②③⑤ | B. | ①③④ | C. | ③④⑤ | D. | ④⑤⑥ |
7.某药物中间体X的结构如图所示,下列说法正确的是( )


| A. | 该X的分子式为C23H25N2O3 | |
| B. | 每个X分子中含有2个手性碳原子 | |
| C. | 1 mol X最多能与9 mol H2发生加成反应 | |
| D. | X能发生水解、氧化和消去反应 |
19.下列说法正确的是( )
| A. | 对于有气体参与的化学平衡体系,增大压强,反应速率一定加快 | |
| B. | 常温下,反应4Fe(OH)2(S)+2H2O(l)+O2(g)=4Fe(OH)3(S)的△H<0,△S<0 | |
| C. | 用0.1mol/L醋酸滴定0.lmol/L NaOH溶液至中性时:c(CH3COO -)+c(CH3COOH)<c(Na+) | |
| D. | 向纯水中加入盐类物质,有可能促进水的电离平衡,但不可能抑制水的电离 |

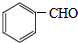
 $\stackrel{KMnO_{4}/H+}{→}$RCOOH+
$\stackrel{KMnO_{4}/H+}{→}$RCOOH+
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O
+H2O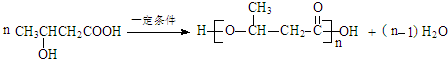 .
. .
. .
.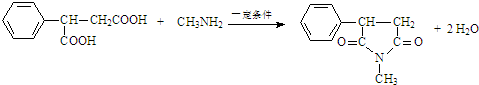 .
.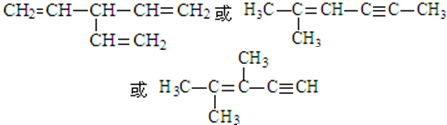 (写出一种即可).
(写出一种即可).
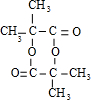 .
. ;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.
;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.
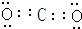 ,Z与氢元素形成的化合物溶于水后,溶液的pH>7(填“<”、“>”或“=”).
,Z与氢元素形成的化合物溶于水后,溶液的pH>7(填“<”、“>”或“=”). ).
).
 .
. .
. .
. 、
、 、
、 .
.