题目内容
10.短周期元素X、Y、Z、W、M的原子序数依次增大,X、Z同主族,Z、W、M同周期,其中X和Y能形成两种物质,且常温下均为液体.W的氧化物既能溶于强碱溶液,又能溶于X、M形成的水溶液.已知W与M形成的物质在178℃时升华.下列说法不正确的是( )| A. | Z、W、M的原子半径由大到小的顺序为Z>W>M | |
| B. | M分别与Z、W所形成的物质的晶体类型相同 | |
| C. | X2Y2易溶于X2Y中,是由于X2Y2与X2Y能形成分子间氢键 | |
| D. | 将Z2Y在空气中加热可得到Z2Y2 |
分析 短周期元素X、Y、Z、W、M的原子序数依次增大,其中X与Y能形成两种物质,且常温下均为液体,可推知X为H元素、Y为O元素;X、Z同主族,Z原子序数大于氧,则Z为Na元素;Z、W、M同周期,处于第三周期,W的氧化物既能溶于强碱溶液,又能溶于X、M形成的水溶液,考虑该氧化物具有两性,W与M形成的物质在178℃时升华,该物质属于分子晶体,则W应为Al,M为Cl,验证符合,据此解答.
解答 解:短周期元素X、Y、Z、W、M的原子序数依次增大,其中X与Y能形成两种物质,且常温下均为液体,可推知X为H元素、Y为O元素;X、Z同主族,Z原子序数大于氧,则Z为Na元素;Z、W、M同周期,处于第三周期,W的氧化物既能溶于强碱溶液,又能溶于X、M形成的水溶液,考虑该氧化物具有两性,W与M形成的物质在178°C时升华,该物质属于分子晶体,则W应为Al,M为Cl,验证符合.
A.同周期随原子序数增大原子半径减小,故原子半径Z(Na)>W(Al)>M(Cl),故A正确;
B.M分别与Z、W所形成的物质为NaCl、AlCl3,前者属于离子晶体、后者属于分子晶体,二者晶体类型不同,故B错误;
C.由于H2O2与H2O能形成分子间氢键,H2O2易溶于H2O中,故C正确;
D.将Na2O在空气中加热,可以与氧气反应生成Na2O2,故D正确,
故选B.
点评 本题考查结构性质位置关系综合应用,推断元素是解题关键,注意对元素化合物性质的掌握及应用.

练习册系列答案
相关题目
1.已知在热的碱性溶液中,Cl2发生如下反应:Cl2+NaOH→NaCl+NaClO3+H2O(未配平).请推测NaClO2在热的碱性溶液中发生反应的最终产物是( )
| A. | NaCl、NaClO | B. | NaCl、NaClO3 | C. | NaClO、NaClO3 | D. | NaClO3、NaClO4 |
18.甲醇是一种可再生能源,又是一种重要的化工原料,具有开发和应用的广阔前景.
工业上可用如下方法合成甲醇:
(1)已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
③H2O(l)═H2O(g)△H=+44.0kJ•mol-1
则甲醇不完全燃烧生成CO和液态水的热化学反应方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
(2)方法一生产甲醇是目前工业上常用的方法.在一定温度下,向2L密闭容器中充入1molCO和2molH2,发生上述反应,5分钟反应达平衡,此时CO的转化率为80%.请回答下列问题:
①前5分钟内甲醇的平均反应速率为0.08mol/(L•min);已知该反应在低温下能自发进行,则反应的△H为<(填“>”、“<”或“=”)0.
②在该温度下反应的平衡常数K=100.
③在图甲方框的坐标系中画出甲醇的物质的量浓度随时间的变化曲线.

(画在答题纸上)
④关于上述反应,下列叙述不正确的是A(填编号).
A.达到平衡时,移走部分甲醇,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(CO)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入0.8molCO和0.6mol CH3OH,则此时v正>v逆
(3)方法二生产甲醇应更具前景,写出方法二生产甲醇的一个优点减少二氧化碳的排放,有效控制温室效应.
(4)根据反应2CH3OH(g)?CH3OCH3(g)+H2O(g),可利用CH3OH生产CH3OCH3.
有人对甲醇脱水转化为二甲醚过程从温度、液体空速(在单位时间内单位体积的催化剂表面通过的原料的量,空速越小,停留时间越长,反应程度越高,但处理能力越小)、压力对甲醇的转化率影响进行研究,分别获得图乙2幅图.
根据以上两幅图选择不受空速影响的合适反应温度和压强320℃、0.2-0.6Mpa.
(5)根据文献,甲醇生产二甲醚的转化率可以根据冷凝的液相中的甲醇与水的相对百分含量来计算(忽略挥发到气相的甲醇).若以Cw表示冷凝液中水的质量分数,CM表示冷凝液中甲醇的质量分数,则甲醇的转化率xM=$\frac{32C{\;}_{W}}{32C{\;}_{W}+9C{\;}_{M}}$.
工业上可用如下方法合成甲醇:
| 方法一 | CO(g)+2H2(g)?CH3OH(g) |
| 方法二 | CO2(g)+3H2(g)?CH3OH(g)+H2O(g) |
②2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
③H2O(l)═H2O(g)△H=+44.0kJ•mol-1
则甲醇不完全燃烧生成CO和液态水的热化学反应方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
(2)方法一生产甲醇是目前工业上常用的方法.在一定温度下,向2L密闭容器中充入1molCO和2molH2,发生上述反应,5分钟反应达平衡,此时CO的转化率为80%.请回答下列问题:
①前5分钟内甲醇的平均反应速率为0.08mol/(L•min);已知该反应在低温下能自发进行,则反应的△H为<(填“>”、“<”或“=”)0.
②在该温度下反应的平衡常数K=100.
③在图甲方框的坐标系中画出甲醇的物质的量浓度随时间的变化曲线.

(画在答题纸上)
④关于上述反应,下列叙述不正确的是A(填编号).
A.达到平衡时,移走部分甲醇,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(CO)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入0.8molCO和0.6mol CH3OH,则此时v正>v逆
(3)方法二生产甲醇应更具前景,写出方法二生产甲醇的一个优点减少二氧化碳的排放,有效控制温室效应.
(4)根据反应2CH3OH(g)?CH3OCH3(g)+H2O(g),可利用CH3OH生产CH3OCH3.
有人对甲醇脱水转化为二甲醚过程从温度、液体空速(在单位时间内单位体积的催化剂表面通过的原料的量,空速越小,停留时间越长,反应程度越高,但处理能力越小)、压力对甲醇的转化率影响进行研究,分别获得图乙2幅图.
根据以上两幅图选择不受空速影响的合适反应温度和压强320℃、0.2-0.6Mpa.
(5)根据文献,甲醇生产二甲醚的转化率可以根据冷凝的液相中的甲醇与水的相对百分含量来计算(忽略挥发到气相的甲醇).若以Cw表示冷凝液中水的质量分数,CM表示冷凝液中甲醇的质量分数,则甲醇的转化率xM=$\frac{32C{\;}_{W}}{32C{\;}_{W}+9C{\;}_{M}}$.
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1 mol•L-1NaClO溶液中含有的ClO-数目为NA | |
| B. | 常温常压下,11.2 L Cl2含氯原子数为NA | |
| C. | 一定条件下,将1 mol N2和3 mol H2混合,充分反应后转移的电子数为6NA | |
| D. | 6.4 g由S2、S4、S8组成的混合物含硫原子数为0.2 NA |
15.向BaCl2溶液中通入物质的量之比为1:2的某混合气体,无沉淀产生,则该混合气体是( )
| A. | Cl2和SO2 | B. | CO2和NH3 | C. | NO和SO2 | D. | NO2和SO2 |
2. 一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )
一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )
 一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )
一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )| A. | T1>T2,该反应的△H>0 | |
| B. | 加入催化剂可以提高CO的转化率 | |
| C. | T1时的平衡常数K1>T2时的平衡常数K2 | |
| D. | CO(g)+2H2(g)?CH3OH(1)的△H值将变大 |
19.下列说法正确的是( )
| A. | 粗锌与稀硫酸反应比纯锌快,说明粗锌中含有更活泼的金属 | |
| B. | 新制氯水显酸性,滴加少量紫色石蕊溶液,溶液始终呈红色 | |
| C. | 常温下,弱酸酸式盐NaHA的pH=6,说明HA-的电离程度大于其水解程度 | |
| D. | 一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的△H<0,△S>0 |
20.下列实验、现象及相关结论均正确的是( )
| A | B | C | D | |
| 实验 | 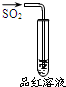 | 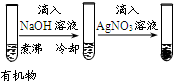 |  | 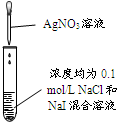 |
| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 | 出现白色沉淀 |
| 结论 | SO2有强氧化性 | 有机物中含有溴原子 | 滴定达到终点 | Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
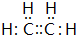 ,A的结构简式H2C=CH2.
,A的结构简式H2C=CH2. ,写出B的一种含三键且无支链的链烃的结构简式CH≡C-CH=CH-CH=CH2.
,写出B的一种含三键且无支链的链烃的结构简式CH≡C-CH=CH-CH=CH2.