题目内容
【题目】目前,人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是________
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是________![]() 填字母代号
填字母代号![]() 。
。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.2V逆(NO2)=V正(N2)
D.容器内混合气体密度保持不变
(2)用活性炭还原法也可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g)△H时,反应进行到不同时间测得各物质的量浓度如下表所示:
N2(g)+CO2(g)△H时,反应进行到不同时间测得各物质的量浓度如下表所示:
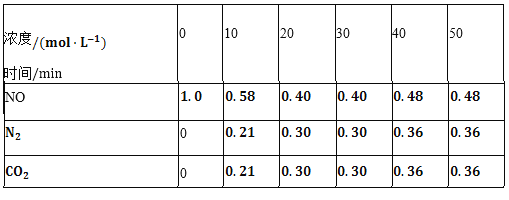
①根据表中数据分析T1℃时,该反应在0~20min的平均反应速率v(CO2)________;计算该反应的平衡常数![]() ________。
________。
②根据上表数据判断,由30min到40min时改变的条件可能是________![]() 任写一种
任写一种![]() 。
。
③若30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,此时NO的转化率________![]() 填“升高”或“降低”
填“升高”或“降低”![]() ,△H________
,△H________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() 。(3)以
。(3)以![]() 与
与![]() 为原料可合成化肥尿素化学式为
为原料可合成化肥尿素化学式为![]() 。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5kJ/mol②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5kJ/mol,③H2O(l)=H2O(g)△H=+44.0kJ/mol,写出CO2与NH3合成尿素和液态水的热化学方程式_____
。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5kJ/mol②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5kJ/mol,③H2O(l)=H2O(g)△H=+44.0kJ/mol,写出CO2与NH3合成尿素和液态水的热化学方程式_____
【答案】A、B 0.015molL-1min-1 0.56(或![]() ) 通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳 降低
) 通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳 降低 ![]()
![]() ΔH=-87kJmol-1
ΔH=-87kJmol-1
【解析】
(1)反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量浓度等不再发生变化;
(2)①由化学反应速率和化学平衡常数公式计算可得;
②由表数据可知40min时,反应的平衡常数与30min中相同,由此分析影响化学平衡移动因素;
③由题给数据可知NO的转化率为![]() ×100%=60%,由30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3计算NO的转化率,判断平衡移动方向;
×100%=60%,由30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3计算NO的转化率,判断平衡移动方向;
(3)由盖斯定律计算可得。
(1)A. 恒温恒容条件下,容器内混合气体颜色不再变化说明二氧化氮的浓度不变,说明正逆反应速率相等,反应达到平衡状态,故正确;
B. 该反应是反应前后气体体积有变化的反应,容器中的压强不再发生变化,说明正逆反应速率相等,反应达到平衡状态,故正确;
C.2V逆(NO2)=V正(N2)说明正逆反应速率不相等,反应没有达到平衡状态,故错误;
D.该反应是反应前后都是气体的反应,由质量守恒定律可知,反应前后气体质量不变,容器恒温恒容条件下,容器的体积不变,容器内混合气体密度始终保持不变,则容器内混合气体密度保持不变不能说明正逆反应速率相等,不能判断反应是否达到平衡状态,故错误;
AB正确,故答案为:AB;
(2)①由表中数据可知0~20min內二氧化碳的浓度变化量为0.30mol/L,则v(CO2)= ![]() =0.015molL-1min-1;20min分钟时反应达到平衡,平衡时各物质的浓度分别为c(N2)=0.3mol/L、c(CO2)=0.3mol/L、c(NO)=0.4mol/L,则反应的平衡常数K=
=0.015molL-1min-1;20min分钟时反应达到平衡,平衡时各物质的浓度分别为c(N2)=0.3mol/L、c(CO2)=0.3mol/L、c(NO)=0.4mol/L,则反应的平衡常数K=![]() =
=![]() =
=![]() ≈0.56,故答案为:0.015molL-1min-1;0.56(或
≈0.56,故答案为:0.015molL-1min-1;0.56(或![]() );
);
②由表数据可知40min时,反应的平衡常数K=![]() =
=![]() ,平衡常数不变说明改变的条件一定不是温度,依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳,故答案为:通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳;
,平衡常数不变说明改变的条件一定不是温度,依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳,故答案为:通入一定量NO或适当缩小容器体积或者充入一定量1:1的氮气和二氧化碳;
③由题给数据可知NO的转化率为![]() ×100%=60%,若30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,设此时NO的转化率为2x,由题意建立如下三段式:
×100%=60%,若30min后升高温度至T2℃,达到新平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,设此时NO的转化率为2x,由题意建立如下三段式:
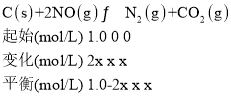
由容器中NO、N2、CO2的浓度之比为5:3:3可得(1.0—2x):x=5:3,解得2x=![]() <60%;温度升高NO的转化率减小,平衡向逆反应方向移动,该反应为放热反应,ΔH<0,故答案为:降低;<;
<60%;温度升高NO的转化率减小,平衡向逆反应方向移动,该反应为放热反应,ΔH<0,故答案为:降低;<;
(3)由盖斯定律可知,①+②—③可得CO2与NH3合成尿素和液态水的热化学方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=△H1+△H2—△H3=(-159.5kJ/mol)+(+116.5kJ/mol)—(+44.0kJ/mol)=-87.0kJ/mol,则热化学方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0kJ/mol,故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0kJ/mol。

 习题精选系列答案
习题精选系列答案