题目内容
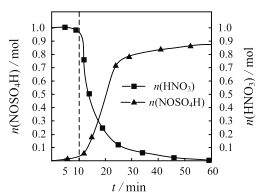
【题目】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室制备亚硝酰硫酸的方法如下:将SO2通入盛有浓硫酸和浓硝酸的混合液中,维持体系温度略低于20℃,搅拌,使其充分反应。反应过程中,亚硝酰硫酸的物质的量和硝酸的物质的量随时间的变化如图所示。
(1)①实验室制备NOSO4H的化学反应方程式为___。
②反应进行到10min后,反应速度明显加快,其可能的原因是___。
③反应过程中,硝酸减少的物质的量大于NOSO4H生成的物质的量的可能原因是___
(2)为了测定亚硝酰硫酸的纯度,进行如下实验:。
准确称取1.200g产品放入锥形瓶中,加入50.00mL0.1000mol·L-1的KMnO4标准溶液和足量稀H2SO4,摇匀,使其充分反应。再将反应后溶液加热至60~70℃(使生成的HNO3挥发逸出),冷却至室温,用0.2500mol·L-1Na2C2O4标准溶液滴定至终点,消耗Na2C2O4溶液的体积为16.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4;KMnO4在酸性条件下被还原为Mn2+。
根据以上实验数据计算亚硝酰硫酸的纯度。(写出计算过程)___
【答案】HNO3+SO2![]() NOSO4H 生成的NOSO4H对该反应有催化作用 硝酸会挥发和分解 90.00%
NOSO4H 生成的NOSO4H对该反应有催化作用 硝酸会挥发和分解 90.00%
【解析】
(1)设NOSO4H中N的化合价为x,根据化合价代数和为0有:x+(+6)×1+(-2)×5+(+1) ×1=0,解得:x=+3,N元素化合价从+5降低到+3,必有S元素化合价从+4升高到+6,发生的是氧化还原反应,氧化剂与还原剂物质的量之比=1:1;
(2)50.00mL0.1000mol·L-1的KMnO4与16.00mL 0.2500mol·L-1Na2C2O4反应之后剩余的KMnO4再与NOSO4H反应。
(1)①N元素化合价从+5降低到+3,必有S元素化合价从+4升高到+6,N元素和S元素的物质的量之比=1:1,所以反应的方程式为:HNO3+SO2 NOSO4H,故答案为:HNO3+SO2
NOSO4H,故答案为:HNO3+SO2 NOSO4H;
NOSO4H;
②反应前十分钟没有加快,不是温度,十分钟后明显加快,说明生成的物质对反应有催化作用,故答案为:生成的NOSO4H对该反应有催化作用;
③从反应的方程式看:参加反应的硝酸和生成的NOSO4H比例为1:1,消耗的硝酸多,可能是有一部分挥发和分解了,故答案为:硝酸会挥发和分解;
(2)一部分KMnO4标准溶液和NOSO4H反应,剩余的KMnO4标准溶液用Na2C2O4反滴定,KMnO4和Na2C2O4,KMnO4中Mn元素化合价从+7降低到+2,降低5,作氧化剂,Na2C2O4中C元素化合价从+3升高到+4升高了1,2个C升高了2,作还原剂,根据得失电子守恒,氧化剂和还原剂的物质的量之比=2:5,所以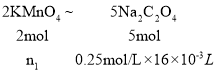 ,解得:和Na2C2O4反应的KMnO4的物质的量n1=1.6×10-3mol,KMnO4总的物质的量=50.00×10-3L×0.1000mol·L-1=5×10-3mol,所以和NOSO4H反应的KMnO4的物质的量=5×10-3mol-1.6×10-3mol=3.4×10-3mol,所以
,解得:和Na2C2O4反应的KMnO4的物质的量n1=1.6×10-3mol,KMnO4总的物质的量=50.00×10-3L×0.1000mol·L-1=5×10-3mol,所以和NOSO4H反应的KMnO4的物质的量=5×10-3mol-1.6×10-3mol=3.4×10-3mol,所以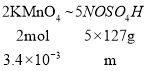 ,解得NOSO4H的质量m=1.0795g,所以样品中NOSO4H的纯度=
,解得NOSO4H的质量m=1.0795g,所以样品中NOSO4H的纯度=![]() ≈90.00%,故答案为:90.00%。
≈90.00%,故答案为:90.00%。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案【题目】下列离子方程式的书写及评价,均合理的是
选项 | 离子方程式 | 评价 |
A | 用铜电极电解饱和KCl溶液:2H2O+2Cl- | 正确:Cl-的失电子能力比OH-强 |
B | 向CuSO4溶液中通入过量的H2S气体:Cu2++H2S=CuS↓+2H+ | 错误:H2S的酸性比H2SO4弱 |
C | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3- +OH- ═BaCO3↓+H2O | 错误:Ba2+与HCO3-系数比应为1:2 |
D | 过量SO2通入到NaClO溶液中:SO2+ClO- +H2O= HClO+HSO3- | 正确:H2SO3的酸性比HClO强 |
A.AB.BC.CD.D
【题目】已知25℃时有关弱电解质的电离平衡常数:
弱电解质化学式 | CH3COOH | NH3·H2O | H2CO3 |
电离平衡常数(25℃) | 1.8×10-5 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
在25℃时,下列有关电解质溶液的说法不正确的是
A.pH相等的四种溶液a. CH3COONa b.Na2CO3 c. NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d<b<c<a
B.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.1L 0.50mol·L-1NH4Cl溶液与2L0.25mo·L-1NH4Cl溶液,前者含NH4+物质的量多
D.浓度均为0.1mol·L-1的CH3COOH、CH3 COONa混合溶液中: c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)
【题目】已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)可逆反应FeO(s)+CO(g)Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表
T/K | 938 | 1100 |
K | 0.68 | 0.40 |
若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态、若降低温度,混合气体的平均相对分子质量__________________;充入氮气,混合气体的密度__________________(填“增大”“减小”或“不变”)。
(2)常温下,浓度均为0.1mol·的下列五种溶液的pH如下表
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,水解能力最弱的是__________________。
②根据表中数据判断,浓度均为0.01mol·L-1的下列四种物质的溶液分别稀释100倍,pH变化最小的是_______(填编号)
A. HClO B. HCN C.H2CO3 D. CH3COOH
③据上表数据,请你判断下列反应不能成立的是_______(填编号)
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
④要增大氯水中HClO的浓度,可向氯水中加入碳酸氢钠,反应的离子方程式为______________
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与CrO42-生成砖红色沉淀指示到达滴定终点当溶液中Cl恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为_______mol·L-1,此时溶液中c(CrO42-)等于_______mol·L-1.(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)