题目内容
6.某固体混合物可能含有Al、NH4Cl、MgCl2、Al2(SO4)3、FeCl2中的一种或几种,现取该混合物进行如下实验: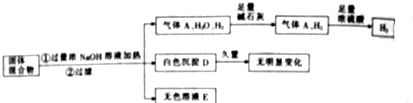
已知气体经过碱石灰和浓硫酸时,二者质量均增大,请回答下列问题:
(1)碱石灰的作用是干燥气体A,气体A是NH3,生成气体A的离子方程式为NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)写出生成H2的反应离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)判断混合物中是否存在FeCl2,并说明理由:白色沉淀D久置颜色无明显变化,说明不存在FeCl2.
(4)白色沉淀D为Mg(0H)2(填化学式,下同);不能确定固体混合物中是否存在的物质是Al2(SO4)3.
分析 固体与浓氢氧化钠反应后生成气体A,通过碱石灰干燥后再经过浓硫酸,浓硫酸质量增大,说明生成NH3,则一定含有NH4Cl,经过浓硫酸后还剩余气体C,则说明生成H2,一定含有Al,得到白色沉淀D,且久置无颜色变化,说明含有MgCl2,不含有FeCl2,生成沉淀为Mg(0H)2,实验不能确定是否含有Al2(SO4)3,以此来解答.
解答 解:固体与浓氢氧化钠反应后生成气体A,通过碱石灰干燥后再经过浓硫酸,浓硫酸质量增大,说明生成NH3,则一定含有NH4Cl,经过浓硫酸后还剩余气体C,则说明生成H2,一定含有Al,得到白色沉淀D,且久置无颜色变化,说明含有MgCl2,不含有FeCl2,生成沉淀为Mg(0H)2,实验不能确定是否含有Al2(SO4)3;
(1)碱石灰具有吸水性,可用于吸收气体中的水蒸气,通过碱石灰干燥后再经过浓硫酸,浓硫酸质量增大,说明气体A为NH3,则一定含有NH4Cl,生成A的离子反应为NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案为:干燥气体A;NH3;NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;
(2)经过浓硫酸后还剩余气体C,则说明生成H2,一定含有Al,生成氢气的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)白色沉淀D久置无颜色变化,说明含有MgCl2,不含有FeCl2,如生成氢氧化亚铁,会迅速变成灰绿色,最终变成红褐色,
故答案为:白色沉淀D久置颜色无明显变化,说明不存在FeCl2;
(4)得到白色沉淀D,且久置无颜色变化,说明含有MgCl2,不含有FeCl2,生成沉淀D为Mg(0H)2,由上述分析可知,不能确定的物质为Al2(SO4)3,
故答案为:Mg(0H)2;Al2(SO4)3.
点评 本题考查无机物的推断,为高频考点,把握元素化合物知识、发生的反应及现象为解答的关键,侧重分析、推断能力的综合考查,题目难度中等.

| A. | 向溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| B. | 一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中,充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 0.01mol•L-1NH4Al(SO4)2溶液与0.02mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | CO(g)的燃烧热是283.0 kJ•mol-1,则CO2分解的热化学方程式为:2CO2(g)=2CO(g)+O2(g)△H=+283.0 kJ•mol-1 |
| A. | 1×10-5mol/L | B. | 1×10-6mol/L | C. | 1×10-8mol/L | D. | 1×10-9molL |

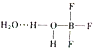 硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.
硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用. )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内最多