题目内容
【题目】已知25℃时Ksp(BaSO4)=1.0×1010。该温度下,CaSO4悬浊液中c(Ca2+)与c(SO42)的关系如图所示,下列叙述正确的是( )

A.向a点的溶液中加入等物质的量固体Na2SO4或Ca(NO3)2,析出的沉淀量不同
B.a、b、c、d四点对应的体系中,d点体系最稳定
C.升高温度后,溶液可能会由a点转化为b点
D.反应Ba2+(aq) + CaSO4(s)![]() BaSO4(s) + Ca2+(aq)的平衡常数K=9×104
BaSO4(s) + Ca2+(aq)的平衡常数K=9×104
【答案】D
【解析】
A、向a点的溶液中加入等物质的量固体Na2SO4或Ca(NO3)2,抑制固体溶解的作用和效果相同,则析出的沉淀量相同,故A错误;
B、曲线上的点为平衡点,c为不饱和溶液,d为过饱和溶液,则d点体系最不稳定,故B错误;
C、a点转化为b点,c(Ca2+)减小、c(SO42)增大,而升高温度,c(Ca2+)与c(SO42)浓度变化趋势相同,则升高温度不能使溶液由a点转化为b点,故C错误;
D、反应Ba2+(aq) + CaSO4(s)![]() BaSO4(s) + Ca2+(aq)的平衡常数K=
BaSO4(s) + Ca2+(aq)的平衡常数K=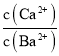 =
=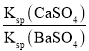 =
=![]() =9×104,故D正确。
=9×104,故D正确。

 智慧小复习系列答案
智慧小复习系列答案【题目】下表列出了A-F6种元素在周期表中短周期的位置。
C | D | ||||||
A | B | E | F |
请回答下列问题:
(1)C元素在周期表中的位置___;C元素的一种氧化物是温室气体,该氧化物的电子式为:___。
(2)A和B的最高价氧化物对应的水化物碱性较强的是___;(填化学式)
(3)D与同族下一周期元素的气态氢化物的沸点较高的是___(填化学式),原因是___。
(4)元素E与元素F相比,非金属性较强的是___(用元素符号填写),下列表述中能证明这一事实的是___(可多选)。
①F的氢化物比E的氢化物稳定
②常温下F的单质和E的单质状态不同
③一定条件下F和E的单质都能与氢氧化钠溶液反应
④F的氧化物的水化物的酸性比E的氧化物的水化物的酸性强
⑤F可以把E从其氢化物水溶液中置换出来
(5)元素E的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式___。