题目内容
【题目】实验室需配制0.2000molL﹣1Na2S2O3标准溶液450mL,并利用该溶液对某浓度的NaClO溶液进行标定.
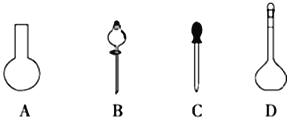
(1)若用Na2S2O3固体来配制标准溶液,在如图所示的仪器中,不必要用到的仪器是_________(填字母),还缺少的玻璃仪器是_________(填仪器名称)。
(2)根据计算需用天平称取Na2S2O3固体的质量是_________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度_________(填“>”“<”或“=”,下同)0.2000molL﹣1.若还未等溶液冷却就定容了,则所得溶液浓度_________0.2000molL﹣1。
(3)用滴定法标定的具体方法:量取20.00mL NaClO溶液于锥形瓶中,加入适量稀盐酸和足量KI固体,用0.2000molL﹣1Na2S2O3标准溶液滴定至终点(淀粉溶液作指示剂),四次平行实验测定的V(Na2S2O3)数据如下:
(已知:I2+2Na2S2O3═2NaI+Na2S4O6)
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
V(Na2S2O3)/mL | 21.90 | 18.80 | 22.10 | 22.00 |
①NaClO溶液中加入适量稀盐酸和足量KI固体时发生反应的离子方程式为_________。
②NaClO溶液的物质的量浓度是_________。
【答案】AB 烧杯、玻璃棒 15.8 = > ClO﹣+2I﹣+2H+═Cl﹣+I2+H2O 0.1100 mol/L
【解析】
(1)用Na2S2O3固体来配制标准溶液,不需要圆底烧瓶、分液漏斗;溶解Na2S2O3固体,还需要烧杯、玻璃棒;
故答案为AB;烧杯、玻璃棒;
(2)配制0.2000molL﹣1Na2S2O3标准溶液450mL,实验室没有450mL的容量瓶,应选用500mL的容量瓶,需要Na2S2O3固体,n=0.2000mol/L×0.5L=1.000mol,m=1.000mol×158g/mol=15.8g;
定容时,还需要向容量瓶中加入蒸馏水,若容量瓶用蒸馏水洗涤后未干燥,不会产生误差;未等溶液冷却就定容了,冷却后,溶液体积减小,所得溶液浓度偏大;
故答案为15.8;=;>;
(3)①NaClO溶液中加入适量稀盐酸和足量KI固体时发生氧化还原反应,其离子方程式为ClO﹣+2I﹣+2H+═Cl﹣+I2+H2O;
②第二次数据明显偏小,不能采用,其余3次平行实验测定的平均体积为:V(Na2S2O3)=![]() =22.00mL,
=22.00mL,
设NaClO溶液的浓度是x,根据反应ClO﹣+2I﹣+2H+═Cl﹣+I2+H2O、I2+2Na2S2O3═2NaI+Na2S4O6
可得关系式:NaClO~2Na2S4O6
1 2
20mL×c 0.2000mol/L×22.00mL
解得:c=0.1100mol/L,
故答案为ClO﹣+2I﹣+2H+═Cl﹣+I2+H2O;0.1100mol/L。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案