题目内容
17.110ml氮气和130mL氢气在一定条件下合成氨,当达到平衡时混合气体的总体积变为220mL,则生成氨气多少mL(请用体积差量法做).分析 N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,反应中4mol的气体生成2mol氨气,气体的体积减少2mol积,据此计算.
解答 解:设生成的氨气为VmL,
N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$ 2NH3,△n
4mol 2mol 2mol
(110+130)mL VmL (110+130-220)mL
则 $\frac{2mol}{VmL}$=$\frac{2mol}{(110+130-220)mL}$,解得V=20mL;
答:生成氨气为20mL.
点评 本题考查了有关方程式的计算,题目难度不大,注意把握差量法在计算中的应用.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
5.下列有机物其一氯代物的结构可能只有一种的是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
12.关于下列图示的说法中正确的是( )
| A. |  用图1装置除去HCl中少量的Cl2 | |
| B. |  用图2装置蒸干Al2(SO4)3饱和溶液制取无水Al2(SO4)3 | |
| C. |  图3制备并收集少量NO2 | |
| D. |  图4是原电池装置,Fe电极为阴极 |
9.为达到预期的实验目的,下列方法可行的是( )
| A. | 用溶解、过滤的方法提纯含有少量碳酸镁的氢氧化镁 | |
| B. | 向混有乙酸的乙酸乙酯中加入NaOH溶液再分液提纯乙酸乙酯 | |
| C. | 除去FeCl2中少量的FeBr2:加入适量氯水,在加四氯化碳萃取、分液 | |
| D. | 向AlCl3溶液中滴加氨水,产生白色沉淀,再加入NaHSO4溶液,沉淀消失 |
6.已知丙烷的燃烧热△H=-2215kJ•mol-1.若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为( )
| A. | 55kJ | B. | 220kJ | C. | 550kJ | D. | 1108kJ |
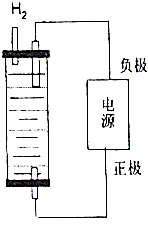 制取漂白粉的氯气通过电解饱和食盐水得到.
制取漂白粉的氯气通过电解饱和食盐水得到. 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量;O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量;O3氧化烟气中SO2、NOx的主要反应的热化学方程式为: