��Ŀ����
7�� ��������Ҫ��Ⱦ��SO2��NOx����O3Ԥ��������CaSO3ˮ����Һ���գ��ɼ���������SO2��NOx�ĺ�����O3����������SO2��NOx����Ҫ��Ӧ���Ȼ�ѧ����ʽΪ��
��������Ҫ��Ⱦ��SO2��NOx����O3Ԥ��������CaSO3ˮ����Һ���գ��ɼ���������SO2��NOx�ĺ�����O3����������SO2��NOx����Ҫ��Ӧ���Ȼ�ѧ����ʽΪ��NO��g��+O3��g���TNO2��g��+O2��g����H=-200.9kJ��mol-1
NO��g��+$\frac{1}{2}$O2��g���TNO2��g����H=-58.2kJ��mol-1
SO2��g��+O3��g���TSO3��g��+O2��g����H=-241.6kJ��mol-1
��1����Ӧ3NO��g��+O3��g��=3NO2��g���ġ�H=-317.3mol•L-1��
��2�������£��̶����뷴Ӧ����NO��SO2�����ʵ������ı����O3�����ʵ�������Ӧһ��ʱ�����ϵ��n��NO����n��NO2����n��SO2���淴Ӧǰn��O3����n��NO���ı仯��ͼ��
�ٵ�n��O3����n��NO����1ʱ����Ӧ��NO2�����ʵ������٣���ԭ����O3��NO2����Ϊ����̬�������
������n��O3����O3����SO2�ķ�Ӧ��������Ӱ�죬�����ԭ���ǿ������䷴Ӧ������
��3������CaSO3ˮ����Һ���վ�O3Ԥ����������ʱ����Һ��pHԼΪ8����SO32-��NO2ת��ΪNO2-�������ӷ���ʽΪ��SO32-+2NO2+2OH-=SO42-+2NO2-+H2O��
��4��CaSO3ˮ����Һ�м���Na2SO4��Һ���ﵽƽ�����Һ��c��SO32-��=$\frac{{K}_{sp}��CaS{O}_{3}��}{{K}_{sp}��CaS{O}_{4}��}��c��S{{O}_{4}}^{2-}��$[��c��SO42-����Ksp��CaSO3����Ksp��CaSO4����ʾ]��CaSO3ˮ����Һ�м���Na2SO4��Һ�����NO2���������ʣ�����Ҫԭ��CaSO3ת��ΪCaSO4ʹ��Һ��SO32-��Ũ�����ӿ�SO32-��NO2�ķ�Ӧ���ʣ�
���� ��1��NO��g��+O3��g���TNO2��g��+O2��g����H=-200.9kJ��mol-1��
NO��g��+$\frac{1}{2}$O2��g���TNO2��g����H=-58.2kJ��mol-1��
������ʽ2��+��3NO��g��+O3��g��=3NO2��g�����ʱ������Ӧ�ĸı䣻
��2���ٳ�������ǿ�����ԣ����������ɵ�NO2��
������n��O3����O3����SO2�ķ�Ӧ��������Ӱ�죬˵��Ũ�ȶԷ�Ӧ����Ӱ���С���������䷴Ӧ���ʽ�����
��3����ҺpHԼΪ8��˵����Һ�ʼ��ԣ�SO32-��NO2ת��ΪNO2-��ͬʱSO32-����������SO42-�����ݷ�Ӧ�����������д���ӷ���ʽ��
��4��CaSO3ˮ����Һ�м���Na2SO4��Һ��������ӦCaSO3+SO42-=CaSO4+SO32-����Һ��c��Ca2+��=$\frac{{K}_{sp}��CaS{O}_{3}��}{c��S{{O}_{3}}^{2-}��}$=$\frac{{K}_{sp}��CaS{O}_{4}��}{c��S{{O}_{4}}^{2-}��}$������CaSO3+SO42-=CaSO4+SO32-֪�����������Ƶ��������������Ũ������Ũ��Խ��Ӧ����Խ��
��� �⣺��1��NO��g��+O3��g���TNO2��g��+O2��g����H=-200.9kJ��mol-1 ��
NO��g��+$\frac{1}{2}$O2��g���TNO2��g����H=-58.2kJ��mol-1��
������ʽ2��+��3NO��g��+O3��g��=3NO2��g�������ԡ�H=2����-58.2kJ��mol-1��+��-200.9kJ��mol-1��=-317.3kJ/mol��
�ʴ�Ϊ��-317.3��
��2���ٵ�n��O3����n��NO����1ʱ��������������������ǿ�����ԣ��ܽ���Ӧ��NO2����Ϊ���۵���������¶����������٣��ʴ�Ϊ��O3��NO2����Ϊ����̬�������
������n��O3����O3����SO2�ķ�Ӧ��������Ӱ�죬˵��Ũ�ȶԷ�Ӧ����Ӱ���С���������䷴Ӧ���ʽ������ʴ�Ϊ���������䷴Ӧ������
��3����ҺpHԼΪ8��˵����Һ�ʼ��ԣ�SO32-��NO2ת��ΪNO2-��ͬʱSO32-����������SO42-�����ݷ�Ӧ�����������д���ӷ���ʽΪSO32-+2NO2+2OH-=SO42-+2NO2-+H2O���ʴ�Ϊ��SO32-+2NO2+2OH-=SO42-+2NO2-+H2O��
��4��CaSO3ˮ����Һ�м���Na2SO4��Һ��������ӦCaSO3+SO42-=CaSO4+SO32-����Һ��c��Ca2+��=$\frac{{K}_{sp}��CaS{O}_{3}��}{c��S{{O}_{3}}^{2-}��}$=$\frac{{K}_{sp}��CaS{O}_{4}��}{c��S{{O}_{4}}^{2-}��}$������c��SO32-��=$\frac{{K}_{sp}��CaS{O}_{3}��}{{K}_{sp}��CaS{O}_{4}��}��c��S{{O}_{4}}^{2-}��$������CaSO3+SO42-=CaSO4+SO32-֪�����������Ƶ���c��SO32-������Ũ��Խ��Ӧ����Խ�����Լӿ췴Ӧ���ʣ����NO2���������ʣ�
�ʴ�Ϊ��$\frac{{K}_{sp}��CaS{O}_{3}��}{{K}_{sp}��CaS{O}_{4}��}��c��S{{O}_{4}}^{2-}��$��CaSO3ת��ΪCaSO4ʹ��Һ��SO32-��Ũ�����ӿ�SO32-��NO2�ķ�Ӧ���ʣ�
���� ����Ϊ2015�꽭��ʡ�߿��⣬�������ܶȻ��������㡢��Ӧ����Ӱ�����ء�������ԭ��Ӧ���ӷ���ʽ����д����˹���ɵ�֪ʶ�㣬�ۺ��Խ�ǿ�����ؿ���ѧ����������������֪���������ʵ����ʡ����ӷ���ʽ��д�����ѵ��ǣ�4������㣬��Ŀ�Ѷ��еȣ�

| A�� |  1��2��4-���ױ� | B�� |  3-����ϩ | C�� |  2-��-1-���� | D�� |  1��3-������� |
| A�� | ����ʽΪC2H6O���л�������������ͬ | |
| B�� | ��ͬ�����£���������̼��a��b����;����ȫת����;��a��;��b�ų��������� ;��a��C$��_{����}^{H_{2}O}$CO+H2$��_{ȼ��}^{O_{2}}$CO2+H2O ;��b��C$��_{ȼ��}^{O_{2}}$CO2 | |
| C�� | ��������ԭ��Ӧ�У���ԭ��ʧȥ�������������������õ����ӵ����� | |
| D�� | ͨ����ѧ�仯����ֱ�ӽ�ˮת��Ϊ���� |
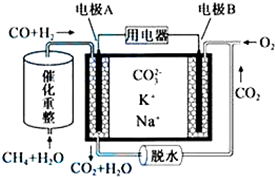
| A�� | ��ӦCH4+H2O$\frac{\underline{����}}{��}$3H2+CO��ÿ����1molCH4ת��12mol���� | |
| B�� | �缫A��H2����ĵ缫��ӦΪ��H2+2OH--2e-=2H2O | |
| C�� | ��ع���ʱ��CO32-��缫B�ƶ� | |
| D�� | �缫B�Ϸ����ĵ缫��ӦΪ��O2+2CO2+4e-=2CO32- |

�ٰ���ͼ���Ӻ�װ�ã����װ�������ԣ�
�ڳ�ȡ���� Fe2O3��ʯӢ�Թ��У���ȼ�ƾ��ƣ�����������ᣮ
�������ij�������ȼ���������ƾ��ƣ�
��30min��Ϩ��ƾ��ƣ��رյ��ɼУ�
�ݴ�������ȴ�����º��ռ����
�������Ϸ����ֱ��ռ����������־ƾ��ƣ��������ֿ��Լ��л��桢����¶ȣ��;ƾ���Ƽ��ȵIJ��
��ش��������⣺
��1���Ʊ�CO��ԭ�������ü��ᣨHCOOH����Ũ������������µķֽ��Ƶã�ʢ�ż������������Ϊ��Һ©�����÷�Ӧ�Ļ�ѧ����ʽHCOOH $��_{��}^{Ũ����}$CO��+H2O��
��2��ʵ�鲽���ij�������ָ����CO���ȣ�
��3��ʵ�鲽���Ϩ��ƾ��Ƶ�˳��Ϊ��I��II�������
��4��ͨ�������ϻ�ȡ������Ϣ��
�ƾ���ƽ���¶�Ϊ600�棻�����־ƾ���ƽ���¶�Ϊ700�棬�ƾ����ƽ���¶�Ϊ930�森
������ָ������Ӧ�¶ȸ���710�棬Fe���ȶ����ڣ�680�桫710��֮�䣬FeO�ȶ����ڣ�����680�棬����Ҫ��Fe3O4���Է����ƾ��Ƽ�������������Fe��ԭ���dz�ʱ�伯�м���ʹ�ֲ��¶ȴﵽ��ԭ����������Ҫ���¶ȣ�
��5����֪FeO��Fe2O3��Fe3O4��Ԫ�ص����������ֱ�Ϊ��22.2%��30%��27.6%��
���������������3����Ʒ����Ԫ�������Ԫ�ص������������±���
| ���ȷ�ʽ | ����Ԫ����� | ��Ԫ�ص���������% | |
| Fe | O | ||
| �ƾ��� | Fe��O | 74.50 | 25.50 |
| �����־ƾ��� | Fe��O | 76.48 | 23.52 |
| �ƾ���� | Fe | 100.00 | 0.00 |
��6��ͨ����һ���������������ǰ���ּ��ȷ�ʽ�õ��Ĺ����ĩ�ɷ־�ΪFe3O4��Fe���þƾ���Ƽ��ȵõ��Ĺ����ĩ�ɷ�ΪFe����������þƾ��Ƽ��ȷ�ʽ�������Fe3O4��Fe��������Ϊ12��1����Ҫ����������
| A�� | LiAlH4��HԪ�صĻ��ϼ�Ϊ-1 | |
| B�� | LiAlH4L��iAlO2��LiH�������ӻ����� | |
| C�� | 1mol LiAlH4��125����ȫ�ֽ⣬ת��4mol���� | |
| D�� | 0.5 mol LiAlH4��ˮ��ַ�Ӧ�����44.8L H2 |

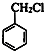 ��C
��C ��
��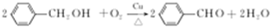 ��
��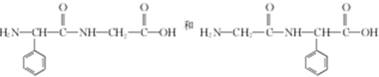 ��
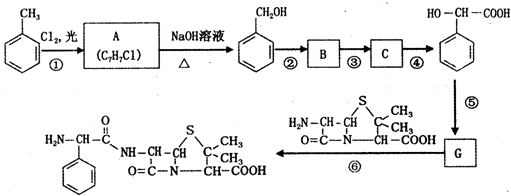
�� ������������ͬ���칹��Ľṹ��ʽ��
������������ͬ���칹��Ľṹ��ʽ�� ��
��