题目内容
14.下列说法正确的是( )| A. | 相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 | |
| B. | 苯和乙醇均不能使酸性高锰酸钾溶液褪色 | |
| C. | 红外光谱分析不能区分乙醇和乙酸乙酯 | |
| D. | 蛋白质、纤维素、蔗糖、淀粉都是高分子化合物 |
分析 A.醇中含-OH,分子之间易形成氢键;
B.乙醇能被强氧化剂氧化;
C.红外光谱可确定有机物中的化学键、官能团;
D.蔗糖的相对分子质量在10000以下,在10000以上的为高分子.
解答 解:A.醇中含-OH,分子之间易形成氢键,则相对分子质量相近的醇比烷烃沸点高,故A正确;
B.乙醇能被酸性高锰酸钾溶液氧化使其褪色,而苯不能,故B错误;
C.红外光谱可确定有机物中的化学键、官能团,则红外光谱分析能区分乙醇和乙酸乙酯,故C错误;
D.蔗糖的相对分子质量在10000以下,不属于高分子,而蛋白质、纤维素、淀粉都是高分子化合物,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列共价化合物中所有原子都满足最外层8电子结构的是( )
| A. | 五氯化磷(PCl5) | B. | 次氯酸(HClO) | C. | 氯化硫(S2Cl2) | D. | 白磷(P4) |
9.下列物质中既能使溴水褪色,也能使高锰酸钾酸性溶液褪色的是( )
| A. | 对二甲苯 | B. | 丙烯 | C. | 丙炔 | D. | 溴乙烷 |
19.当前在人类已知的化合物中,品种最多的是( )
| A. | ⅤA 族元素的化合物 | B. | ⅢB族元素的化合物 | ||
| C. | 过渡元素的化合物 | D. | ⅣA 族元素的化合物 |
6.下列物质中,既能发生取代反应,又能发生消去反应,同时催化氧化生成醛的是( )
| A. |  | B. |  | C. | CH3OH | D. |  |
3.如图为番茄电池,下列说法正确的是( )
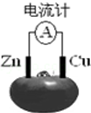

| A. | 锌电极为电池的正极 | |
| B. | 铜电极发生氧化反应 | |
| C. | 工作一段时间后,锌片质量会减轻 | |
| D. | 电池工作时,铜电极附近会出现蓝色 |
4.化学用语在化学学习中有着重要的作用.下列有关化学用语使用正确的是( )
| A. | CO2的电子式 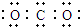 | B. | Cl-的结构示意图 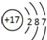 | ||
| C. | HCl的电子式 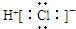 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基. .
. 已知磺酰氯(SO2Cl2)是一种有机氯化剂,SO2(g)+Cl2(g)=SO2C12(g)△H<0,SO2Cl2是一种无色液体,熔点-54.1℃,沸点69.1℃,极易水解,遇潮湿空气会产生白雾.
已知磺酰氯(SO2Cl2)是一种有机氯化剂,SO2(g)+Cl2(g)=SO2C12(g)△H<0,SO2Cl2是一种无色液体,熔点-54.1℃,沸点69.1℃,极易水解,遇潮湿空气会产生白雾.