题目内容
19.当前在人类已知的化合物中,品种最多的是( )| A. | ⅤA 族元素的化合物 | B. | ⅢB族元素的化合物 | ||
| C. | 过渡元素的化合物 | D. | ⅣA 族元素的化合物 |
分析 A、ⅤA族元素的化合物主要为氧化物、酸、盐及某些氢化物;
B、ⅢB族元素的化合物,为金属元素;
C、过渡元素的化合物,为金属化合物;
D、ⅣA族元素的化合物除氧化物、酸、盐之外,形成的有机化合物已超过3000万种.
解答 解:A、ⅤA族元素的化合物主要为氧化物、酸、盐及某些氢化物,化合物中品种有限,故A不选;
B、ⅢB族元素的化合物,为金属元素,主要应用在金属材料及催化剂等的选择,故B错误;
C、过渡元素的化合物,为金属化合物,化合物中品种有限,故C错误;
D、ⅣA族元素的化合物除氧化物、酸、盐之外,形成的有机化合物已超过3000万种,化合物品种最多,故D选;
故选D.
点评 本题考查常见的化合物的种类,明确有机物在人类生活、生产中的重要应用是解答本题的关键,题目难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
10.下列实验现象描述或说法不正确的是( )
| A. | 标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量的浓度为$\frac{1}{22.4}$ mol/L | |
| B. | 氨很容易液化,因此氨常用作制冷剂 | |
| C. | SO3溶于水能导电,所以SO3是电解质 | |
| D. | 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
7.在 2L密闭容器中发生反应N2+3H2?2NH3,经一段时间后NH3 的物质的量增加了2.4mol,这段时间内用氢气表示的反应速率为0.6mol/(L•s),则这段时间为( )
| A. | 6 s | B. | 4 s | C. | 3 s | D. | 2 s |
14.下列说法正确的是( )
| A. | 相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 | |
| B. | 苯和乙醇均不能使酸性高锰酸钾溶液褪色 | |
| C. | 红外光谱分析不能区分乙醇和乙酸乙酯 | |
| D. | 蛋白质、纤维素、蔗糖、淀粉都是高分子化合物 |
8.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 元素的电负性 C>D>A>B |
9.下列物质中可用作光导纤维的是( )
| A. | 单晶硅 | B. | 石英 | C. | 陶瓷 | D. | 水玻璃 |
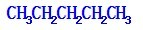 、
、 、
、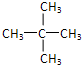 .
.