题目内容
4.化学用语在化学学习中有着重要的作用.下列有关化学用语使用正确的是( )| A. | CO2的电子式 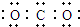 | B. | Cl-的结构示意图 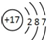 | ||
| C. | HCl的电子式 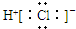 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |
分析 A、二氧化碳中C分别与2个O形成共价键;
B、氯离子的核电荷数为17,核外电子总数为18,最外层为8个电子;
C、氯化氢为共价化合物,分子中存在一个氢氯共用电子对,氯原子最外层一个为8个电子;
D、元素符号的左上角表示的是质量数,应该为37,左下角为质子数.
解答 解:A、二氧化碳中C分别与2个O形成共价键,二氧化碳的电子式为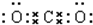 ,故A错误;
,故A错误;
B、氯离子的核电荷数为17,核外电子总数为18,最外层为8个电子,氯离子正确的结构示意图为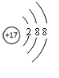 ,故B错误;
,故B错误;
C、氯化氢属于共价化合物,分子中存在一个H-Cl键,氯原子最外层达到8个电子,氯化氢正确的电子式为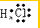 ,故C错误;
,故C错误;
D、氯元素的核电荷数为17,质量数为37的氯原子可以表示为:1737Cl,故D正确;
故选D.
点评 本题考查了电子式、离子结构示意图、元素符号、结构式等化学用语的判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确离子结构示意图与原子结构示意图的区别.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
14.下列说法正确的是( )
| A. | 相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 | |
| B. | 苯和乙醇均不能使酸性高锰酸钾溶液褪色 | |
| C. | 红外光谱分析不能区分乙醇和乙酸乙酯 | |
| D. | 蛋白质、纤维素、蔗糖、淀粉都是高分子化合物 |
15.某主族元素最外层只有1个电子,则该元素一定是( )
| A. | ⅠA族元素 | B. | +7价元素 | C. | 三周期元素 | D. | 金属元素 |
12. 在一密闭容器中有如下反应:L(s)+aG(g)═bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
在一密闭容器中有如下反应:L(s)+aG(g)═bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
 在一密闭容器中有如下反应:L(s)+aG(g)═bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
在一密闭容器中有如下反应:L(s)+aG(g)═bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )| A. | 正反应为放热反应 | B. | 化学方程式中的计量数a>b | ||
| C. | G的转化率随温度升高而减小 | D. | 增大压强,容器内气体的质量变大 |
19.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 4.0 g重水(D2O)中所含质子数为0.4NA | |
| B. | 4.48 L N2与CO的混合物中所含分子数为0.2NA | |
| C. | 6.2 g白磷与红磷的混合物中所含磷原子数为0.2NA | |
| D. | 12.5 mL 16 mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
9.下列物质中可用作光导纤维的是( )
| A. | 单晶硅 | B. | 石英 | C. | 陶瓷 | D. | 水玻璃 |
16.下列关于主族元素的叙述,不正确的是( )
| A. | 元素原子的最外层电子数等于主族族序数 | |
| B. | 都既有正化合价、又有负化合价 | |
| C. | 元素的最高正价数不一定等于原子最外层电子数 | |
| D. | 最低负价数的绝对值等于原子形成稳定结构所需电子数 |
13. 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示.下列叙述中,正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示.下列叙述中,正确的是( )
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示.下列叙述中,正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图所示.下列叙述中,正确的是( )| A. | 该反应的化学方程式为2 M?N | |
| B. | t1时N的浓度是M浓度的2倍 | |
| C. | t2时正逆反应速率相等,反应达到平衡状态 | |
| D. | t3时正反应速率大于逆反应速率 |
14.下列物质中既能脱水生成烯烃又能催化氧化生成醛的是( )
| A. | 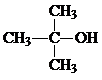 | B. | 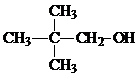 | ||
| C. | 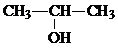 | D. | 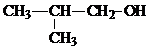 |