题目内容
【题目】若将铝粉分别加入下列溶液中,能放出氢气,且可能大量共存的是( )
A.H+、Ba2+、Cl﹣、NO3﹣
B.NH4+、CO3﹣、NO3﹣、Na+
C.NO3﹣、K+、[Al(OH)4]﹣、OH﹣
D.Na+、Ba2+、Mg2+、HCO3﹣
【答案】C
【解析】解:A.溶液中含有NO3﹣ , 与铝反应不生成氢气,故A错误;
B.碱性条件下NH4+不能大量共存,酸性条件下CO3﹣不能大量共存,故B错误;
C.碱性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.无论溶液呈酸性还是碱性,HCO3﹣都不能大量共存,故D错误.
故选C.

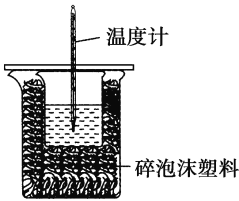
【题目】某实验小组用100 mL 0.50 mol·L-1 NaOH溶液与100 mL 0.55 mol·L-1盐酸进行中和热的测定。装置如图所示。回答下列问题:
(1)若实验共需要400 mL NaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体______g。
(2)图中装置缺少的仪器是______________________________。
(3)盐酸稍过量的原因是________________________________。
(4)碎泡沫塑料及泡沫塑料板的作用是___________________。
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热(ΔH)________(填“偏大”“偏小”或“不变”),其原因是_______。
(6)请填写下表中的平均温度差:
实验次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 平均温度差 (T2-T1)/℃ | |||
HCl | NaOH | 平均值 | ||||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | ||
3 | 25.9 | 25.9 | 25.9 | 29.8 | ||
4 | 26.4 | 26.2 | 26.3 | 30.4 | ||
(7)若测得该反应放出的热量为2.865 kJ,请写出盐酸与NaOH溶液反应的中和热的方程式:__________________________________________。