��Ŀ����
����Ŀ������˹�������ӡ�M�������ػ���ɹ���������������������Ԥ������������õ����ػ��ʹ�õ�����Һ��Ϊȼ�ռ���Һ��Ϊ�������ĸ��ܵ����ƽ�������֪��
��1��H2(g)=H2(l) ��H1=-0.92kJ��mol-1
��2��O2(g)=O2(l) ��H2=-6.84kJ��mol-1
��3����ͼ��
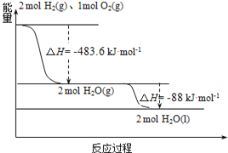
����˵����ȷ���ǣ� ��
A. 2mol H2(g)��1molO2(g)�������������2molH2O(g)�������������
B. �����Һ��ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(l)+O2(l)=2H2O(g) ��H=-474.92kJ��mol-1
C. ������ȼ����Ϊ��H=-241.8kJ��mol-1
D. H2O(g)���H2O(l)�Ĺ����У��ϼ����յ�����С�ڳɼ��ų�������
���𰸡�B
��������
A����ͼ���֪2mol H2��g����1mol O2��g����Ӧ����2mol H2O��g�����ų�483.6kJ����������2mol H2��g����1mol O2��g�������е���������2mol H2O��g�������е��������ߣ�ѡ��A����
B����ͼ���֪2H2��g��+O2��g���T2H2O��g����H=-483.6kJmol-1�٣�H2��g��=H2��l����H1=-0.92kJmol-1�ڣ�O2��g��=O2��l����H2=-6.84kJmol-1�ۣ����ݸ�˹���ɿ�֪����-����2-�ۿɵ�2H2��l��+O2��l���T2H2O��g����H=-474.92kJmol-1��ѡ��B��ȷ��
C��������ȼ������ָ1mol������ȫȼ������Һ̬ˮ�ų�����������������ȼ����Ϊ��H=-��483.6+88��kJ/mol��2��-285.8kJ/mol��ѡ��C����
D��H2O��g�����H2O��l��Ϊ�����仯�������ڻ�ѧ���Ķ��Ѻ����ɣ�ѡ��D����
��ѡB��

 ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�����Ŀ����.ʵ����ѡ������KMnO4��Һ��H2C2O4��Һ��Ӧ��̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
ʵ��ǰ��������KMnO4����Һ�ζ�δ֪Ũ�ȵIJ���
��1����ƽ��Ӧԭ�����ӷ���ʽ��
___MnO4-�� __H2C2O4��___��___Mn2���� ___CO2����____H2O
��2��̽��Ӱ�컯ѧ��Ӧ���ʵ�����
ʵ�� ��� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
Ũ��/mol��L��1 | ���/mL | Ũ��/mol��L��1 | ���/mL | ||
�� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
a.̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_______(���ţ���ͬ)��̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������_______��
b.���Һ��ɫʱ���ɴ�С��˳����_____________��
c.���ij��ʵ��(����)ʱ��Һ��Mn2�����ʵ�����ʱ���ϵ��ͼ��ʾ���������n(Mn2��)�ڷ�Ӧ��ʼʱ�仯����һ��ʱ����������������Ҫԭ��_______��

��. ������KMnO4��Һ�ζ������ʵ�Na2C2O4��Ʒ����֪���ʲ���KMnO4��H2SO4��Һ��Ӧ����
ʵ�鲽�裺ȷȡ1 g Na2C2O4��Ʒ�����
��3�����������ҺӦװ��____�ζ����С���������ʽ��������ʽ����
��4���ζ����յ�ʱ��ʵ�������ǣ�_________��
��5��������Ʒ��Na2C2O4�Ĵ�����______%��
����Ŀ����������Ϊһ�����ʹ��ܵ�أ���Ӧ���õ����Ӻͷ�չ�������������ڽ����ơ�������Ͷ�������Na2SX���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մ����ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ1��ʾ��
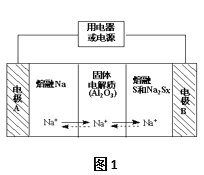
��1�����ݱ����ݣ������жϸõ�ع���������Ӧ����
��_____������ĸ����Χ����
A��100������ B��100��300��
C��300��350�� D��350��2050��
���� | Na | S | Al2O3 |
�۵�/�� | 97.8 | 115 | 2050 |
�е�/�� | 892 | 444.6 | 2980 |
��2���ŵ�ʱ���缫AΪ_____�����缫B����_____��Ӧ������������ԭ������
��3�����ʱ���ܷ�ӦΪNa2Sx��2Na+xS���������ĵ缫��ӦʽΪ��________________��
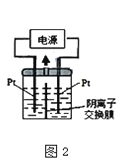
��4��������������Ϊ��Դ��������װ��KI��������Һ��ͼ2��ʾ�����ڵ��м��������ӽ���Ĥ������ͨ��һ��ʱ����������Һ����ɫ��һ��ʱ�����ɫ��dz�����Ҳ���ĵ缫����ʽ��________________���Է��������Һ��ɫ��dz�Ŀ���ԭ���ǣ�___________________��