��Ŀ����
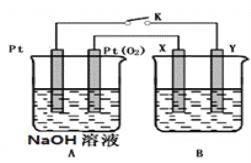
����Ŀ������(C3H8)������ȼ�ϵ�غ�п���ؾ�Ϊ��;�㷺��ֱ����Դ���ŵ�ʱ���ߵ��ܷ�Ӧ�ֱ�ΪC3H8+5O2=3CO2+4H2O��2Zn+O2=2ZnO���ñ���(C3H8)ȼ�ϵ��Ϊп���س���װ����ͼ��ʾ������˵������ȷ����

A. ����MΪCO2
B. ȼ�ϵ������1mo1 O2ʱ����������4 mol OH-��bĤ��P�缫�ƶ�
C. aĤ��bĤ������ѡ�������ӽ���Ĥ
D. ��װ���У�п���صĸ�����ӦʽΪZn+2OH--2e-=ZnO+H2O
���𰸡�D
��������A. ȼ�ϵ�������ڵ���������ڵ�̼���ƣ��������������õ����ӽ��CO2ת��Ϊ̼�����������MΪCO2��A��ȷ��B. ȼ�ϵ������1mo1 O2ʱע��4mol�������������������������ƶ��������������4 mol OH-��bĤ��P�缫�ƶ���B��ȷ��C. ԭ�������������̼���������������Ҫ���̼�������aĤ��bĤ������ѡ�������ӽ���Ĥ��C��ȷ��D. ��װ���У�п���صĸ�����ʱ��Ϊ��������ӦʽΪZnO+H2O+2e-=Zn+2OH-��D����ѡD��

��ϰ��ϵ�д�
 Сѧ��ʱ��ѵϵ�д�
Сѧ��ʱ��ѵϵ�д�
�����Ŀ