题目内容
【题目】A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
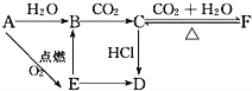
(1)写出A、B、C、D、E、F的化学式:
A.___,B.___,C.___,D.___,E.___,F.___。
(2)写出有关反应的化学方程式(是离子反应的直接写离子方程式)。
A→E:___,
E→B:___,
F→C:___。
【答案】Na NaOH Na2CO3 NaCl Na2O2 NaHCO3 2Na+O2![]() Na2O2 2Na2O2+2H2O=4Na++4OH-+O2↑ 2NaHCO3
Na2O2 2Na2O2+2H2O=4Na++4OH-+O2↑ 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
【解析】
A与氧气在点燃条件下反应生成淡黄色粉末E,则E为Na2O2,A为Na,钠与水反应生成B且B也能由过氧化钠转化得到,可推知B为NaOH,由NaOH与二氧化碳反应得到C,C与二氧化碳、水反应得到F,可推知C为Na2CO3、F为NaHCO3,碳酸钠与HCl反应得到D,且D也能由过氧化钠转化得到,可推知D为NaCl,据此解答。
(1)由上述分析可知,A为Na,B为NaOH,C为Na2CO3,D为NaCl,E为Na2O2,F为NaHCO3,
故答案为:Na;NaOH;Na2CO3;NaCl;Na2O2;NaHCO3;
(2)Na与氧气在点燃条件下反应生成Na2O2,其反应不是离子反应,因此其化学反应方程式为:2Na+O2![]() Na2O2;
Na2O2;
过氧化钠与水反应生成氢氧化钠、氧气,其反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑;
碳酸氢钠在加热条件下会发生分解反应生成碳酸钠、二氧化碳、水,其反应不是离子反应,因此其化学反应方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,
Na2CO3+H2O+CO2↑,
故答案为:2Na+O2![]() Na2O2;2Na2O2+2H2O=4Na++4OH-+O2↑;2NaHCO3
Na2O2;2Na2O2+2H2O=4Na++4OH-+O2↑;2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。