��Ŀ����
����Ŀ������ת���⡣A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ���£����ַ�Ӧ�е�ˮ����ȥ������������ش��������⣺
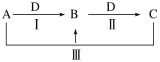
��1����A��B��C����ɫ��Ӧ��Ϊ��ɫ��CΪ�����е���Ʒ��D�Ĺ����ŷŻ��������ЧӦ��
��A�Ļ�ѧʽ______________��B������____________��
�ڷ�Ӧ������ӷ���ʽ��_____________��
��2����A��D��Ϊ���ʣ���AΪ���壬DԪ�ص�һ�ֺ���ɫ�����ﳣ�������ϡ�
�ٷ�Ӧ������ӷ���ʽ��____________��
�ڷ�Ӧ������ӷ���ʽ��ʾ��Ӧ__________��
�ۼ���B����������õ��Լ���_________��д��ѧʽ����
��3��C��NaOH��Һ��Ӧ�������ӷ���ʽ��ʾ����������Ĺ���________��_____��
���𰸡�NaOH ������մ� CO32-+CO2+H2O==2HCO3- 2Fe3++Fe��3Fe2+ 2Fe2++Cl2==2Fe3++2Cl- KSCN Fe2++2OH-==Fe(OH)2�� 4Fe(OH)2+O2+2H2O==4Fe(OH)3
��������
��1����A��B��C����ɫ��Ӧ��Ϊ��ɫ������Ԫ�أ�CΪ�����е���Ʒ����C ΪNaHCO3��D�Ĺ����ŷŻ��������ЧӦ����DΪCO2��
�ٲ������Ʒ�����ȷ��A��B��
�ڷ�Ӧ��Ϊ̼�����������̼��ˮ�ķ�Ӧ��
��2����A��D��Ϊ���ʣ���AΪ���壬DԪ�ص�һ�ֺ���ɫ�����ﳣ�������ϣ���DΪFe����AΪCl2��
�ٷ�Ӧ��Ϊ�Ȼ���������Ӧ��
�ڷ�Ӧ��Ϊ�������Ȼ�������Ӧ��
�ۼ���B�������ӣ�������Fe3+����õ��Լ������軯�ء�
��3���Ȼ�������NaOH��Һ��Ӧ���ȷ������ֽⷴӦ������������Ӧ��
��1�������Ϸ�������ȷ��A��B��C�ж�����Ԫ����C ΪNaHCO3��DΪCO2��
�ٲ������Ʒ�����ȷ��BΪNa2CO3����AΪNaOH��B������Ϊ������մ�
��Ϊ��NaOH��������մ�
�ڷ�Ӧ��Ϊ̼�����������̼��ˮ�ķ�Ӧ�����ӷ���ʽΪCO32-+CO2+H2O==2HCO3-��
����CO32-+CO2+H2O==2HCO3-��
��2����A��D��Ϊ���ʣ���AΪ���壬DԪ�ص�һ�ֺ���ɫ�����ﳣ�������ϣ���DΪFe����AΪCl2����BΪFeCl3��CΪFeCl2��
�ٷ�Ӧ��Ϊ�Ȼ���������Ӧ�����ӷ���ʽ��2Fe3++Fe��3Fe2+����Ϊ��2Fe3++Fe��3Fe2+��
�ڷ�Ӧ��Ϊ�������Ȼ�������Ӧ�����ӷ���ʽ��2Fe2++Cl2==2Fe3++2Cl-��
����2Fe2++Cl2==2Fe3++2Cl-��
�ۼ���B�������ӣ�������Fe3+�����������������軯����Һ��������Һ��ΪѪ��ɫ����˼��������ӵ�����Լ���KSCN��
����KSCN��
��3���Ȼ�������NaOH��Һ��Ӧ���ȷ������ֽⷴӦ������������Ӧ������ʽΪFe2++2OH-=Fe(OH)2����4Fe(OH)2+O2+2H2O==4Fe(OH)3��
����Fe2++2OH-=Fe(OH)2����4Fe(OH)2+O2+2H2O==4Fe(OH)3��

����Ŀ��I������(H2C2O4)���������������������ܹ�������Ӧ��
��ʵ��1����ͬѧ��8.00 mL 0.001 mol/L KMnO4��Һ��5.00 mL 0.01 mol/L H2C2O4��Һ��Ӧ���о���ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�졣�ı���������£�
��� | KMnO4��Һ /mL | H2C2O4��Һ /mL | 10%�������/mL | �¶�/�� | �������� |
�� | 8.00 | 5.00 | 3.00 | 20 | |
�� | 8.00 | 5.00 | 3.00 | 30 | |
�� | 8.00 | 5.00 | 1.00 | 20 | 2.00 mL����ˮ |
��1��д������(H2C2O4)����������Һ�����������·�Ӧ�����ӷ���ʽ________��
��2����������ʵ����Ŀ����̽��__________�Ի�ѧ��Ӧ���ʵ�Ӱ�졣
��ʵ��2����ͬѧ���о������������������������·�Ӧ��Ӱ������ʱ����,���������Ը��������Һ��ʼһ��ʱ�䷴Ӧ���ʽ���,��Һ��ɫ������,�����ú�ͻȻ��ɫ,��Ӧ�������Լӿ졣
��3�������������,��ͬѧ��Ϊ�����������ط�Ӧ����,������Һ�¶�����,��Ӧ���ʼӿ졣��Ӱ�컯ѧ��Ӧ���ʵ����ؿ�,����뻹������_______��Ӱ�졣
��4������ʵ��֤����IJ���,�������Ը��������Һ�Ͳ�����Һ��,����Ҫѡ����Լ����������____������ĸ����
a������� b��ˮ c���������� d��������
������ͼ��ʾ��װ�ý����к��ȵIJⶨʵ�飬�ֱ�ȡ![]() ��
��![]() ��Һ��
��Һ��![]() ���������ʵ�飬�ش��������⣺
���������ʵ�飬�ش��������⣺
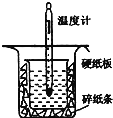
��1������ͼʵ��װ�ÿ���������ȱ�ٵ�һ�ֲ�����Ʒ��__________������֮�⣬װ���е�һ�����Դ�����__________��
��2��������Ϊ![]() ��NaOH��Һ��
��NaOH��Һ��![]() ��������Һ���ܶȶ���
��������Һ���ܶȶ���![]() ���кͺ�������Һ�ı�����
���кͺ�������Һ�ı�����![]() ��ͨ���������ݼ����к��ȡ�H=__________���������С�����һλ����
��ͨ���������ݼ����к��ȡ�H=__________���������С�����һλ����
�¶� ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | ||
H2SO4 | NaOH | ƽ��ֵ | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
��3������ʵ����ֵ�����![]() ��ƫ�����ƫ���ԭ������ǣ�����ĸ��_____��
��ƫ�����ƫ���ԭ������ǣ�����ĸ��_____��
a��ʵ��װ�ñ��¡�����Ч����
b�����¶ȼƲⶨ![]() ��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶�
c���ֶ�ΰ�![]() ��Һ����ʢ�������С�ձ���
��Һ����ʢ�������С�ձ���
d����������ʵ������¶Ⱦ��������ƽ��ֵ
����Ŀ��������X����Y��Һ�У����ɳ������ʵ���n2������X�����ʵ���n1�Ĺ�ϵ��ͼ��ʾ������ͼ��ʾ�������
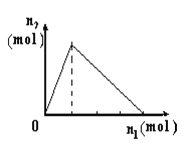
A | B | C | D | |
X | NaOH | AlCl3 | HCl | NaAlO2 |
Y | AlCl3 | NaOH | NaAlO2 | HCl |
A. A B. B C. C D. D