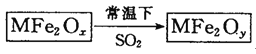题目内容
【题目】研究![]() 等大气污染气体的处理具有重要意义。
等大气污染气体的处理具有重要意义。
(1)已知:![]() ;
;![]() ;
;
则反应![]() 的
的![]() =________。
=________。
(2)一定条件下,将![]() 与
与![]() 以体积比
以体积比![]() 置于密闭容器中发生上述反应,测得上述反应平衡时
置于密闭容器中发生上述反应,测得上述反应平衡时![]() 与
与![]() 体积比为
体积比为![]() ,则平衡常数
,则平衡常数![]() =________(保留两位小数)。
=________(保留两位小数)。
(3)![]() 可用于合成甲醇,反应方程式为
可用于合成甲醇,反应方程式为![]() 。
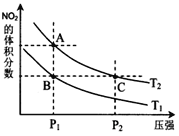
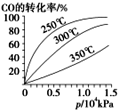
。![]() 在不同温度下的平衡转化率与压强的关系如图所示。该反应
在不同温度下的平衡转化率与压强的关系如图所示。该反应![]() ________
________![]() (填“>”或“<”)。实际生产条件控制在
(填“>”或“<”)。实际生产条件控制在![]() 、
、![]() 左右,选择此压强的理由是__________________。
左右,选择此压强的理由是__________________。
【答案】-41.8 kJ·mol-1 8/3 < 250℃、1.2×104kPa左右,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失
【解析】
(1)已知:![]() ①
①
![]() ②
②
将①-②得:2NO2(g)+2SO2(g)![]() 2SO3(g)+2NO(g) H=-83.6 kJ· mol-1,由此得出NO2(g)+SO2(g)
2SO3(g)+2NO(g) H=-83.6 kJ· mol-1,由此得出NO2(g)+SO2(g)![]() SO3(g)+NO(g) H=-41.8 kJ·mol-1。
SO3(g)+NO(g) H=-41.8 kJ·mol-1。
(2)令NO2的体积为1,则SO2的体积为2。设变化量为x
NO2(g)+SO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
起始量 1 2 0 0
变化量 x x x x
平衡量 1-x 2-x x x
依题意得![]() ,解得x=0.8,由于反应前后体积不变,则
,解得x=0.8,由于反应前后体积不变,则![]() 。
。
(3)由图象信息可知,压强相同时,升高温度,CO的转化率降低,说明升高温度,平衡逆向移动,正反应为放热反应,H<0。因为反应物的气体分子数大于生成物的气体分子数,加压有利于平衡的正向移动,但压强越大需要的条件越高,花费越大,所以选择1.2×104kPa这个压强的原因是由于250℃、1.2×104kPa左右,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失

练习册系列答案
相关题目