题目内容
1.下列有关化学用语使用正确的是( )| A. | NH4Br的电子式: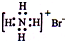 | |
| B. | CO2的比例模型: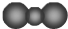 | |
| C. | CCl4分子构型为正四面体,其键与键之间的夹角为109°28′ | |
| D. | 中子数为20的氯原子:20Cl |
分析 A、溴离子电子式书写错误,应画出最外层电子数,用“[]”括起,并在右上角注明所带电荷;
B、二氧化碳分子中C的原子半径大于O原子半径;
C、四氯化碳可以看作甲烷的四个H原子被Cl原子取代生成的产物;
D、原子符号ZAX左下角Z代表质子数,左上角A代表质量数,X代表元素符号,其中质量数=质子数+中子数.
解答 解:A、NH4Br属于离子化合物,由铵根离子与溴离子构成,电子式为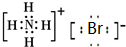 ,故A错误;
,故A错误;
B、二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,正确为 ,故B错误;
,故B错误;
C、CCl4分子中碳原子sp3杂化,没有弧对电子对,所以构型为正四面体,故C正确;
D、原子核内有20个中子的氯原子,其质量数为17+20=37,原子符号为37Cl,故D错误;
故选C.
点评 本题主要考查常用化学用语的书写,难度不大,注意掌握常见有机官能团的结构简式书写,阴离子、复杂阳离子应用“[]”括起,并在右上角注明所带电荷.

练习册系列答案
相关题目
12.(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+6NH3↑+3SO2↑+SO3↑+7H2O,将反应后的混合气体先通过置于冰水浴的U型管,再通入足量的BaCl2溶液,结果为( )
| A. | 产生BaSO4和BaSO3沉淀 | B. | 无沉淀产生 | ||
| C. | 产生BaSO4沉淀 | D. | 产生BaSO3沉淀 |
16.下列说法中正确的是( )
| A. | 球棍模型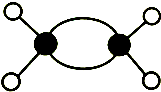 表示的有机物是乙烯 表示的有机物是乙烯 | |
| B. | 电子式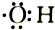 可以表示羟基,也可以表示氢氧根 可以表示羟基,也可以表示氢氧根 | |
| C. | 有机物 的分子式为C6H8O2 的分子式为C6H8O2 | |
| D. | 结构简式(CH3)2CHOH:可以表示1-丙醇,也可以表示2-丙醇 |
10.冬季的降雪给机场和马路带来诸多不便,其中醋酸钾(CH3COOK)是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是( )
| A. | 1 mol CH3COOK的质量为98 g•mol-1 | |
| B. | CH3COOK的摩尔质量等于它的相对分子质量 | |
| C. | 一个CH3COOK微粒的质量约为$\frac{98}{6.02×1{0}^{23}}$g | |
| D. | 含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol |
11.同一温度下,A物质10g溶于50g水中成饱和溶液,B物质的饱和溶液的质量分数为30%,C物质的溶质分别蒸发10g水,第一次析出2g晶体,第二次析出4g晶体,则A、B、C三种物质的溶解度大小顺序为( )
| A. | A>B>C | B. | A<B<C | C. | C>A>B | D. | B>C>A |
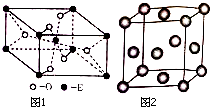 已知A、B、C、D、E五种元素的原子序数依次增大,A元素位于周期表的s区,其原子中电子层数等于未成对电子数;B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂.E是有“生物金属”之称,E4+和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次增大,A元素位于周期表的s区,其原子中电子层数等于未成对电子数;B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂.E是有“生物金属”之称,E4+和氩原子的核外电子排布相同. .
.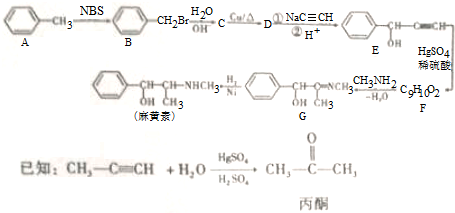

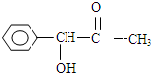 ,H是F的同分异构体,H中含有苯环,苯环上只有两个取代基,并且能发生水解反应,则H的可能结构有12种,其中核磁共振氢谱显示有四组峰的结构简式为(任写~种)
,H是F的同分异构体,H中含有苯环,苯环上只有两个取代基,并且能发生水解反应,则H的可能结构有12种,其中核磁共振氢谱显示有四组峰的结构简式为(任写~种)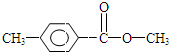 或
或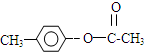 .
.