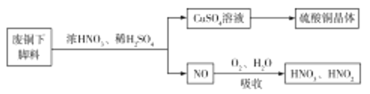
��Ŀ����
����Ŀ��˫��ˮ����Ҫ�Ļ�ѧ�Լ���
(1)һ�������£�O2�õ���ת��Ϊ�������ɻ�(��O![]() )����ʵ������ͼ��ʾ��ת����
)����ʵ������ͼ��ʾ��ת����
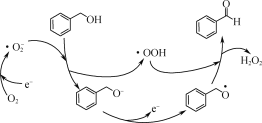
��![]() ��________(����������������ԭ��)��Ӧ��
��________(����������������ԭ��)��Ӧ��
��д��ͼʾת���ܷ�Ӧ�Ļ�ѧ����ʽ��________��
(2) K2Cr2O7������������H2O2��Ӧ����CrO5����ӦΪ��������ԭ��Ӧ���ݴ˷�����CrO5�У�2��O�룭1��O����Ŀ��Ϊ________��
(3) H2O2�����ڲⶨ�ƾ��������Ҵ��ĺ���������20.00 mLij��β�ƣ�������CH3CH2OH������ͨ��17.0 mL 0.200 0 mol��L��1 K2Cr2O7��Һ(H2SO4�ữ)�У�������Ӧ��K2Cr2O7��C2H5OH��H2SO4�D��Cr2(SO4)3��CH3COOH��K2SO4��H2O(δ��ƽ)
����0.400 0 mol��L��1��˫��ˮ�ζ���Ӧ�����õĻ��Һ����ȥ19.00 mL˫��ˮ���ζ������з������·�Ӧ��
��Ӧ1��4H2O2��K2Cr2O7��H2SO4===K2SO4��2CrO5��5H2O
��Ӧ2��H2O2��CH3COOH===CH3COOOH��H2O
��ü�β����CH3CH2OH�����ʵ���Ũ��Ϊ________mol��L��1(д���������)��
���𰸡�����  1:4 0.18 mol��L��1
1:4 0.18 mol��L��1
�輦β���к���C2H5OH�����ʵ���Ϊx mol
K2Cr2O7�������ʵ�����n(K2Cr2O7)��17.00��10��3 L��0.200 0 mol��L��1��3.4��10��3 mol
H2O2�������ʵ�����n(H2O2)��19.00��10��3 L��0.400 0 mol��L��1��7.6��10��3 mol
����2K2Cr2O7��3C2H5OH��8H2SO4===2Cr2(SO4)3��3CH3COOH��2K2SO4��11H2O
![]() x mol���� x mol�� x mol
x mol���� x mol�� x mol
�������
4H2O2�������� �� ��������K2Cr2O7��������������H2SO4===2CrO5��5H2O��K2SO4
4��(3.4��10��3��![]() x) mol�� (3.4��10��3��
x) mol�� (3.4��10��3��![]() x) mol
x) mol
H2O2��CH3COOH===CH3COOOH��H2O
x mol����x mol
���ݡ�4��(3.4��10��3��![]() x)��x��7.6��10��3
x)��x��7.6��10��3
���x��3.6��10��3 mol
c(C2H5OH)��![]() ��3.6��10��3 mol��0.02 L��0.18 mol��L��1
��3.6��10��3 mol��0.02 L��0.18 mol��L��1
��������
(1)��![]() ��һ������ɣ�
��һ������ɣ�![]() �ǵ����Ե�ԭ���ţ����ߺ��е�ԭ�Ӹ�����ȣ����ǰ�߱Ⱥ��ߵ�������1����������
�ǵ����Ե�ԭ���ţ����ߺ��е�ԭ�Ӹ�����ȣ����ǰ�߱Ⱥ��ߵ�������1����������![]() ����
����![]() �ķ�Ӧ��������Ӧ��
�ķ�Ӧ��������Ӧ��
��O2����һ�������µõ���ת��Ϊ�������ɻ������״��ڳ������ɻ��������½����һ��H+�볬�����ɻ����ת��Ϊ![]() ��ͬʱҲ����һ��
��ͬʱҲ����һ��![]() �����
�����![]() ������ʧȥ1������ת��Ϊ
������ʧȥ1������ת��Ϊ![]() ��
��![]() ����
����![]() ��Ӧ��ʹ
��Ӧ��ʹ![]() ��ȥ1��Hԭ���γɱ���ȩ��
��ȥ1��Hԭ���γɱ���ȩ��![]() ����Hԭ�ӽ���γɹ���������ӣ��������ת�����ܷ�Ӧ����ʽΪ��
����Hԭ�ӽ���γɹ���������ӣ��������ת�����ܷ�Ӧ����ʽΪ��![]() +O2
+O2![]()
![]() +H2O2��
+H2O2��
(2)K2Cr2O7�е�CrΪ+6�ۣ���������������������������ⷴӦ����CrO5Ϊ��������ԭ��Ӧ������CrO5�е�CrҲΪ+6�ۣ���ô��CrO5��-2�����ĸ���Ϊx��-1�����ĸ���Ϊy�����У�![]() ��
��![]() �����x=1��y=4�����Ա���Ϊ1:4��
�����x=1��y=4�����Ա���Ϊ1:4��
(3)�ȼ���![]() �������ʵ���Ϊ
�������ʵ���Ϊ![]() ��
��![]() ���ܵ����ʵ���Ϊ
���ܵ����ʵ���Ϊ![]() ���Ҵ�ͨ�������ظ������Һ�з����ķ�Ӧ����ʽ����ȫ����ƽ����Ӧ������1���Ҵ�������Ϊ������Ҫʧȥ4�����ӣ�1���ظ���ر���ԭΪCr2(SO4)3��Ҫ��6�����ӣ���˶��߷�Ӧʱ��
���Ҵ�ͨ�������ظ������Һ�з����ķ�Ӧ����ʽ����ȫ����ƽ����Ӧ������1���Ҵ�������Ϊ������Ҫʧȥ4�����ӣ�1���ظ���ر���ԭΪCr2(SO4)3��Ҫ��6�����ӣ���˶��߷�Ӧʱ��![]() ������20.00mL��β�����Ҵ���xmol����ô��һ����Ӧ���ĵ�
������20.00mL��β�����Ҵ���xmol����ô��һ����Ӧ���ĵ�![]() Ϊ
Ϊ![]() mol���ù�������ζ�ʱ����Ӧ2�е����ἴ���Ҵ���������������Ϊxmol����ô���ݷ�Ӧ����ʽ�������ĵ�
mol���ù�������ζ�ʱ����Ӧ2�е����ἴ���Ҵ���������������Ϊxmol����ô���ݷ�Ӧ����ʽ�������ĵ�![]() �����ʵ���Ϊxmol��
�����ʵ���Ϊxmol��![]() �ڽ��Ҵ�����Ϊ�����ʣ������ʵ���Ϊ
�ڽ��Ҵ�����Ϊ�����ʣ������ʵ���Ϊ![]() ����ôͨ����Ӧ1���ĵ�
����ôͨ����Ӧ1���ĵ�![]() �����ʵ���Ϊ
�����ʵ���Ϊ![]() �������У�
��������![]() �����
�����![]() ����ô��β�����Ҵ���Ũ��Ϊ
����ô��β�����Ҵ���Ũ��Ϊ![]() ��
��

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�����Ŀ������̿�����ڴ���������Ⱦ��NO����1 L�ܱ������м���NO��
����̿(������)����������E��F�����¶ȷֱ���T1���T2��ʱ�����ƽ��ʱ�����ʵ����ʵ������±���
��������������n/mol | ����̿ | NO | E | F |
��ʼ | 2.030 | 0.100 | 0 | 0 |
T1 | 2.000 | 0.040 | 0.030 | 0.030 |
T2 | 2.005 | 0.050 | 0.025 | 0.025 |
(1)�����ϱ����ݣ�д��NO�����̿��Ӧ�Ļ�ѧ����ʽ��___________��
(2)������Ӧ��T1��ʱ��ƽ�ⳣ��ΪK1����T2��ʱ��ƽ�ⳣ��ΪK2��
�ټ���K1��_______________��
�ڸ���������Ϣ�жϣ�T1��T2�Ĺ�ϵ��_______(�����)��
a��T1��T2b��T1��T2c�����Ƚ�
(3)��T1���·�Ӧ�ﵽƽ������д�ʩ���ܸı�NO��ת���ʵ���_______(�����)��
a������c(NO) b������ѹǿ
c�������¶� d����ȥ����F