题目内容
16.某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度.有关的叙述正确的是( )| A. | H2Y的电离方程式为:H2Y+2H2O?2H3O++Y2- | |
| B. | 在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) | |
| C. | HY-的水解方程式为HY-+H2O?H3O++Y2- | |
| D. | 在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+) |
分析 A.A、H2Y是二元弱酸,电离时分两步电离;
B.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小;
C.HY-水解生成二元弱酸和氢氧根离子;
D.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小.
解答 解:A.H2Y是二元弱酸,电离时分两步电离,第一步电离生成氢离子和酸式酸根离子,电离方程式为:H2Y+H2O?HY-+H3O+,故A错误;
B.NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故B错误;
C.HY-水解生成二元弱酸和氢氧根离子,水解方程式为:HY-+H2O?OH-+H2Y,选项中是电离方程式,故C错误;
D.根据B的分析可知:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故D正确;
故选D.
点评 本题考查了溶液中离子浓度大小比较,题目难度中等,明确“HY-的电离程度小于HY-的水解程度”的含义为解答本题的关键,注意掌握电荷守恒、物料守恒、盐的水解原理在判断溶液离子浓度大小中的应用方法.

练习册系列答案
相关题目
7.化学与环境保护密切相关,下列叙述正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 处理废水时加入明矾作为消毒剂对水进行杀菌消毒 | |
| C. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| D. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
4.在25℃时,将0.2mol CH3COONa晶体和0.1mol HCl气体同时溶解于同一烧杯的水中,制得1L溶液,若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是( )
| A. | 该溶液的pH小于7 | B. | c(CH3COOH)+c(CH3COO-)=0.20 mol•L-1 | ||
| C. | c(CH3COO-)+c(OH-)=0.10 mol•L-1 | D. | c(CH3COOH)<c(CH3COO-) |
11.水煤气是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
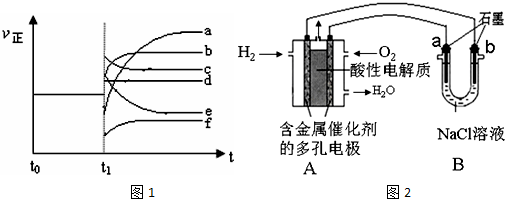
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
(6 )如图2是利用氢氧燃料作电源,用惰性电极电解200ml 1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气4.48L(设电解后溶液体积不变).
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.

C(s)+H2O(g)?CO (g)+H2 (g)△H=+131.3kJ•mol-1
(1)该反应的平衡常数K随温度的升高而增大(增大、减小、不变).
(2)上述反应达到平衡后,增加H2O(g)的量,则C(s)的物质的量减小(增大、减小、不变).
(3)下列说法一定能判断如上反应达平衡的是BD
A.消耗1mol H2O(g)同时生成1mol H2
B.容器内混合气体的总质量不变
C.H2O(g)、CO (g)、H2 (g)三种气体的浓度比为1:1:1
D.恒温恒容时容器内气体的压强不变
(4)上述反应在t0时刻达到平衡,在t1时刻改变某一条件后正反应速率(ν正)随时间的变化如图1所示,
填出对应的编号.
①缩小容器体积b;
②降低温度f;
(5)一定温度下,三个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示.请填写表中①②相应的空格.
| 容器编号 | c(H2O)/mol•L-1 | c(CO)/mol•L-1 | c(H2)/mol•L-1 | ν正、ν逆比较 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ①0.6 | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ②ν正>ν逆 |
①电解后溶液的pH=14(忽略氯气与氢氧化钠溶液反应)
②阳极产生气体的体积在标准状况下是3.36 L.
1.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A. | 正极为Fe,负极为Zn,电解质Fe2(SO4)3溶液 | |
| B. | 正极为Cu,负极为Fe,电解质FeCl3溶液 | |
| C. | 正极为Cu,负极为Fe,电解质Fe(NO3)3溶液 | |
| D. | 正极为Ag,负极为Fe,电解质Fe2(SO4)3溶液 |
8.下列分子式表示的物质一定是纯净物的是( )
| A. | C4H10 | B. | CH2Cl2 | C. | C2H4O2 | D. |  |
5.警察常从案发现场的人体气味来获取有用线索.人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④乙酸乙酯;⑤十八烷;⑥己醛;⑦庚醛.下列说法正确的是( )
| A. | ①、②、⑥分子中碳原子数小于10,③、⑤分子中碳原子数大于10 | |
| B. | ①、②是无机物,③、⑤、⑦是有机物 | |
| C. | ①、④是酸,③、⑤不是酸 | |
| D. | ②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |