题目内容
6.有下列8种晶体:A.水晶 B.冰醋酸 C.白磷 D.固态氩 E.氯化铵 F.铝 G.金刚石
用序号回答下列问题:
(1)属于原子晶体的化合物是A,直接由原子构成的晶体是ADG,直接由原子构成的分子晶体是D.
(2)由存在非极性键晶体是CG,含有共价键的离子晶体是E,属于分子晶体的单质是CD.
(3)在一定条件下能导电而不发生化学反应的是F,分子内存在化学键,但受热熔化时,化学键不发生变化的是BC,受热熔化,需克服共价键的是AG.
分析 (1)原子晶体的构成微粒为原子,分子晶体的构成微粒为分子,但稀有气体形成的分子晶体由原子构成的分子;
(2)存在非极性键晶体是白磷和金刚石,氯化铵是含有共价键的离子晶体,白磷和氩是分子晶体;
(3)金属铝在一定条件下能导电而不发生化学反应,含有共价键的分子晶体,熔化时破坏分子间作用力,不破坏共价键,原子晶体熔化时破坏共价键.
解答 解:(1)水晶、金刚石都是原子晶体,水晶化学成分为二氧化硅,属于原子晶体的化合物,金刚石是单质,所以直接由原子构成的晶体是ADG,直接由原子构成的分子晶体是稀有气体D,
故答案为:A;ADG;D;
(2)由存在非极性键晶体是白磷和金刚石,含有共价键的离子晶体是氯化铵,是分子晶体而且是单质的是白磷和固体氩,
故答案为:CG;E;CD;
(3)金属铝在一定条件下能导电而不发生化学反应,冰醋酸和白磷是含有共价键的分子晶体,熔化时破坏分子间作用力,不破坏共价键,水晶和金刚石属于原子晶体,熔化时破坏共价键,
故答案为:F;BC;AG.
点评 本题考查了化学键的类型和晶体的类型及性质,题目具有一定的综合性,准确判断化学键类型和晶体类型是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度.有关的叙述正确的是( )
| A. | H2Y的电离方程式为:H2Y+2H2O?2H3O++Y2- | |
| B. | 在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) | |
| C. | HY-的水解方程式为HY-+H2O?H3O++Y2- | |
| D. | 在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+) |
17.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: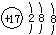 | |
| B. | 作为相对原子质量测定标准的碳核素:12C | |
| C. | 氨气(NH3)中氮元素的化合价是+3 | |
| D. | Na+的电子式:Na+ |
11.W、X、Y、Z为原子序数依次增大的同周期的短周期元素.已知W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水.下列判断正确的是( )
| A. | W、Y、Z三种元素的最高价氧化物的水化物可能有两种是强碱、一种是强酸 | |
| B. | Z元素在第3周期第ⅥA族 | |
| C. | W、Y、Z三种元素有两种是金属、一种是非金属 | |
| D. | W、X、Y三种元素最高价氧化物对应水化物的碱性依次增强 |
18.下列操作能导致置换反应发生的是( )
| A. | 将铜片置于盐酸中 | B. | 将锌片置于MgCl2溶液中 | ||
| C. | 将铁片置于CuSO4溶液中 | D. | Na2CO3 溶液与CaCl2溶液混合 |
15.化学反应的发生必然伴随有能量的转化,其最根本的原因是( )
| A. | 化学反应中一定有新物质生成 | |
| B. | 化学反应中旧的化学键的断裂需要吸收热量,新的化学键的生成需要放出能量 | |
| C. | 化学反应通常需要加热等条件才能发生 | |
| D. | 能量变化是化学反应的基本特征之一 |
16.下列有关物质用途或现象以及反应方程式不正确的是( )
| A. | 汽车尾气中发生的催化转化反应:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2 | |
| B. | 工业制氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O | |
| C. | 燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2 | |
| D. | 用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+CO32-═CaCO3+SO42- |
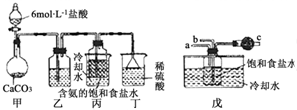 “侯氏制碱法”是我国化工专家侯德榜以NaCl、NH3、CO2等为原料制得NaHCO3,进而生产纯碱的一种化工方法.有关的化学反应方程式如下:
“侯氏制碱法”是我国化工专家侯德榜以NaCl、NH3、CO2等为原料制得NaHCO3,进而生产纯碱的一种化工方法.有关的化学反应方程式如下: