题目内容
【题目】NaH2PO2可用于化学镀镍,常通过反应“P4+3NaOH+3H2O==3NaH2PO2+PH3↑”制得,产物PH3中P的化合价为-3。下列说法正确的是
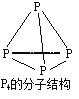
A.P4分子中含有的共价键是极性键
B.31g P4中所含P-P键的物质的量为6 mol
C.反应中还原剂和氧化剂的物质的量之比为1∶3
D.反应生成2.24 L PH3(标准状况),转移电子数目为0.3×6.02×1023
【答案】D
【解析】
A.P4分子中存在PP键,为非极性键,A项错误;
B.1个P4分子含有6个PP键,则31g即0.25mol P4,所含PP键的物质的量为1.5 mol,B项错误;
C. 反应生成NaH2PO2,P的元素化合价从0价变为+1价,生成PH3,P元素化合价由0价降低为3价,可知NaH2PO2为氧化产物,PH3为还原产物,则反应中还原剂和氧化剂的物质的量之比为3:1,C项错误;
D. 生成PH3,P元素化合价由0价降低为3价,则反应生成2.24 L PH3(标准状况),即0.1mol,转移电子数目为0.3×6.02×1023,D项正确;
答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是)
选项 | 已知 | 类推 |
A | 将Fe加入CuSO4溶液中:Fe+Cu2+=== Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+Cu2+=== Cu+2Na+ |
B | 向Ca(ClO)2溶液中通入少量CO2:CO2+H2O+Ca2++2ClO-=== CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:SO2+H2O+Ca2++2ClO-=== CaSO3↓+2HClO |
C | 惰性电极电解氯化钠溶液:2Cl-+2H2O | 惰性电极电解MgBr2溶液:2Br-+2H2O |
D | 稀盐酸与NaOH溶液反应至中性:H++OH-===H2O | 稀硝酸与Ba(OH)2溶液反应至中性:H++OH-===H2O |
A. A B. B C. C D. D