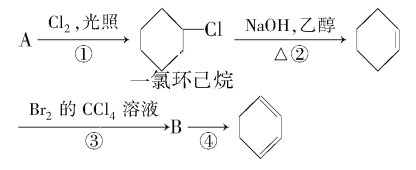
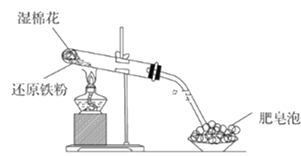
题目内容
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. ![]() 的溶液中:K+、Na+、CO32-、NO3-
的溶液中:K+、Na+、CO32-、NO3-
B.澄清透明的溶液中:Fe3+、Mg2+、SCN-、Cl-
C.c(Fe2+)=1 mol/L的溶液中: Na+、NH4+、AlO2-、SO42-
D.能使甲基橙变红的溶液中: K+、NH4+、SO42-、HCO3-
【答案】A
【解析】
离子之间能够大量共存是指离子之间既不发生反应生成沉淀、气体、水、弱电解质等,也不发生氧化还原反应、络合反应等,据此进行分析解答。
A.![]() 的溶液呈碱性,这几种离子相互间不反应且都不与氢氧根离子反应,所以能大量共存,A选项符合题意;
的溶液呈碱性,这几种离子相互间不反应且都不与氢氧根离子反应,所以能大量共存,A选项符合题意;
B.Fe3+、SCN发生络合反应而不能大量共存,B选项不符合题意;
C.Fe2+、NH4+与AlO2-发生双水解而不能大量共存,C选项不符合题意;
D.能使甲基橙溶液变红色,说明溶液呈酸性,HCO3能和氢离子反应生成二氧化碳和水而不能大量共存,D选项不符合题意;
答案选A。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】如何降低大气中CO2的含量及有效地开发利用碳资源的研究越来越紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
如表所列数据是反应在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断△H ________0 ( 填“>”、 “ < “ 或 “ = ”) ;
②判断反应达到平衡状态的依据是________.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
③借助上表数据判断,要提高CO的转化率,可采取的措施是________.
A.升温 B.充入更多H2 C.分离出甲醇 D.加入催化剂
(2)CH3OH可以用做燃料电池的燃料,以甲醇与氧气的反应为原理设计,现有电解质溶液是KOH溶液的燃料电池。请写出该电池负极的电极反应式:____________________.
(3)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)BaCO3(s)+SO42-(aq)。已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=________________。