题目内容
【题目】无水![]() 广泛用作有机反应催化剂。实验室采用镁屑与液溴为原料制备无水
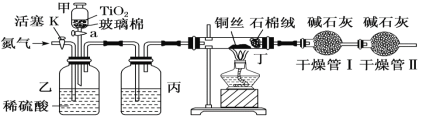
广泛用作有机反应催化剂。实验室采用镁屑与液溴为原料制备无水![]() ,装置如图1,主要步骤如下:
,装置如图1,主要步骤如下:
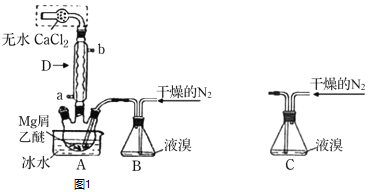
步骤1三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴。
步骤2缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至![]() ,析出晶体,再过滤得三乙醚合溴化镁粗品。
,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4常温下用苯溶解粗品,冷却至![]() ,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至
,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至![]() 分解得无水
分解得无水![]() 产品。
产品。
已知:![]() 和
和![]() 反应剧烈放热;乙醚
反应剧烈放热;乙醚![]() 极易挥发;
极易挥发;
![]() 具有强吸水性。
具有强吸水性。
![]()
![]()
![]()
请回答下列问题:
![]() 仪器D的名称是___________________。冷凝水应该从________
仪器D的名称是___________________。冷凝水应该从________![]() 填a或
填a或![]() 口通入;
口通入;
![]() 干燥的
干燥的![]() 可将液溴吹出,是因为液溴具有___________的性质;实验中不能用干燥空气代替干燥
可将液溴吹出,是因为液溴具有___________的性质;实验中不能用干燥空气代替干燥![]() ,原因是___________;
,原因是___________;
![]() 将装置B改为装置C,可能会导致的后果是_____________________________;
将装置B改为装置C,可能会导致的后果是_____________________________;
![]() 步骤3中,第一次过滤除去的物质是___________________________________;
步骤3中,第一次过滤除去的物质是___________________________________;
![]() 试用平衡移动的原理说明得到三乙醚合溴化镁后,加热有利于其分解,得无水
试用平衡移动的原理说明得到三乙醚合溴化镁后,加热有利于其分解,得无水![]() 产品的原因:__________________________;
产品的原因:__________________________;
![]() 为测定产品的纯度,可用EDTA标准溶液滴定,反应的离子方程式:
为测定产品的纯度,可用EDTA标准溶液滴定,反应的离子方程式:![]() ;测定前,先称取
;测定前,先称取![]() 无水
无水![]() 产品,溶解后,用0.0500mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液20.00mL,则测得无水
产品,溶解后,用0.0500mol/L的EDTA标准溶液滴定至终点,消耗EDTA标准溶液20.00mL,则测得无水![]() 产品的纯度是_________________
产品的纯度是_________________![]() 以质量分数表示
以质量分数表示![]() 。
。
【答案】球形冷凝管 a 极易挥发 镁屑会与空气中的氧气反应,生成的MgO阻碍反应的继续进行 会将液溴挤压入三颈瓶中,反应加剧大量放热存在安全隐患 镁屑 加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动 ![]()
【解析】
(1)根据仪器构造,D为球形冷凝管;冷凝水应该从a口通入;故答案为:球形冷凝管; a;
(2)干燥的![]() 可将液溴吹出,是因为液溴具有极易挥发的性质;实验中不能用干燥空气代替干燥
可将液溴吹出,是因为液溴具有极易挥发的性质;实验中不能用干燥空气代替干燥![]() ,原因是镁屑与氧气反应生成的氧化镁阻碍Mg和
,原因是镁屑与氧气反应生成的氧化镁阻碍Mg和![]() 的反应;
的反应;
故答案为:极易挥发;镁屑会与空气中的氧气反应,生成的MgO阻碍反应的继续进行;
(3)将装置B改为C装置,当干燥的氮气通入,会使气压变大,将液溴快速压入三颈瓶,反应过快大量放热存在安全隐患,装置B是利用干燥的氮气将溴蒸气带入三颈瓶中,反应容易控制,防止反应过快。
故答案为:会将液溴快速压入三颈瓶,反应过快大量放热而存在安全隐患;
(4)步骤3过滤除去的是未反应的镁屑。
故答案为:镁屑;
(5)加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动;故答案为:加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动;
(6)依据方程式Mg2++EDTA=EDTA—Mg2+分析,溴化镁的物质的量![]() ,则溴化镁的质量为
,则溴化镁的质量为![]() ,溴化镁的产品的纯度
,溴化镁的产品的纯度![]() 。
。
故答案为:![]() 。
。

【题目】根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是 ( )
选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
A | SO2 | sp | 直线形 | 直线形 |
B | H2O | sp2 | 平面三角形 | V形 |
C | NH3 | sp2 | 三角锥形 | 三角锥形 |
D | CH4 | sp3 | 正四面体形 | 正四面体形 |
A.AB.BC.CD.D