题目内容
【题目】氰化钠![]() 是重要的化工原料,易溶于水,易水解生成氰化氢,剧毒物质。常用于电镀、冶金、有机合成医药、络合剂和掩蔽剂。
是重要的化工原料,易溶于水,易水解生成氰化氢,剧毒物质。常用于电镀、冶金、有机合成医药、络合剂和掩蔽剂。
![]() 装氰化钠
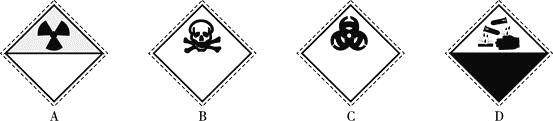
装氰化钠![]() 试剂瓶的标签上应印有下列警示标记中的________
试剂瓶的标签上应印有下列警示标记中的________![]() 填序号
填序号![]() 。
。
![]() 实验室用NaCN固体配制NaCN溶液时,为避免其水解,应先将其溶于______________浓溶液,再用蒸馏水稀释。
实验室用NaCN固体配制NaCN溶液时,为避免其水解,应先将其溶于______________浓溶液,再用蒸馏水稀释。
![]() 泄漏时用双氧水处理以减轻环境污染,处理后生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的离子方程式是__________________________________________。
泄漏时用双氧水处理以减轻环境污染,处理后生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的离子方程式是__________________________________________。
![]() 化学兴趣小组利用:2NH
化学兴趣小组利用:2NH![]() 反应原理制备NaCN并检测其纯度。
反应原理制备NaCN并检测其纯度。
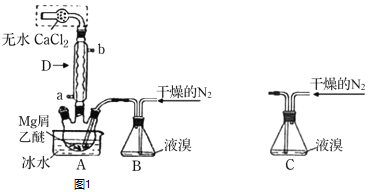
实验一:制备NaCN装置如图所示
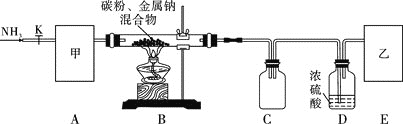
![]() 装置C的作用是____________。甲可选取下列装置中的________
装置C的作用是____________。甲可选取下列装置中的________![]() 填序号
填序号![]() 。
。

![]() 安装好实验仪器,检查装置气密性,取一定量的碳粉与金属钠混合,放入硬质玻璃管内;接下来的操作正确的是________
安装好实验仪器,检查装置气密性,取一定量的碳粉与金属钠混合,放入硬质玻璃管内;接下来的操作正确的是________![]() 填序号
填序号![]() 。
。
A.先打开活塞K,缓缓通入一段时间氨气后再加热硬质玻璃管
B.先加热硬质玻璃管,再打开活塞K,缓缓通入氨气
C.打开活塞K,一边缓缓通入氨气,同时加热硬质玻璃管
![]() 上述装置中乙处还需补充的实验仪器或装置有__________________。
上述装置中乙处还需补充的实验仪器或装置有__________________。
实验二:测定产品中氰化钠的含量
![]() 已知: Ag
已知: Ag![]() ,Ag
,Ag![]() ,AgI呈黄色,且CN
,AgI呈黄色,且CN![]() 优先与Ag
优先与Ag![]() 反应。取制备好的产品
反应。取制备好的产品![]() ,配成
,配成![]() 溶液,取
溶液,取![]() 于锥形瓶中,并滴加
于锥形瓶中,并滴加![]() 滴KI溶液作指示剂,用
滴KI溶液作指示剂,用![]() 的标准AgNO
的标准AgNO![]() 溶液滴定3次,平均消耗AgNO
溶液滴定3次,平均消耗AgNO![]() 溶液的体积为
溶液的体积为![]() 。滴定终点的现象是____________________________________________________________,产品氰化钠的纯度为________
。滴定终点的现象是____________________________________________________________,产品氰化钠的纯度为________![]() 。
。
【答案】![]()
![]()
![]() 作安全瓶,防止倒吸 c
作安全瓶,防止倒吸 c ![]() 氢气储气瓶
氢气储气瓶![]() 气球、酒精灯等合理答案均给分
气球、酒精灯等合理答案均给分![]() 滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失
滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失 ![]() 或
或![]()
【解析】
![]() 氰化钠
氰化钠![]() 是剧毒物质,故选B;
是剧毒物质,故选B;
![]() 氰化钠
氰化钠![]() 是强碱弱酸盐,水解显碱性,为避免其水解,应先将其溶于NaOH浓溶液,再用蒸馏水稀释,故答案为:NaOH;
是强碱弱酸盐,水解显碱性,为避免其水解,应先将其溶于NaOH浓溶液,再用蒸馏水稀释,故答案为:NaOH;
![]() 用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,即反应生成了
用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,即反应生成了![]() 和
和![]() ,离子方程式为
,离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
![]() 由于氨气极易溶于水,使体系内压强快速减小,易发生倒吸,所以C装置是安全瓶,防止倒吸,甲是干燥氨气的装置,选碱石灰,故答案为:作安全瓶,防止倒吸;c;
由于氨气极易溶于水,使体系内压强快速减小,易发生倒吸,所以C装置是安全瓶,防止倒吸,甲是干燥氨气的装置,选碱石灰,故答案为:作安全瓶,防止倒吸;c;
![]() 防止Na与空气中的成分反应,应先通气体排尽装置中的空气后加热,故选A;
防止Na与空气中的成分反应,应先通气体排尽装置中的空气后加热,故选A;
![]() 乙处还需补充的实验仪器或装置是收集氢气的装置,故答案为:氢气储气瓶
乙处还需补充的实验仪器或装置是收集氢气的装置,故答案为:氢气储气瓶![]() 气球、酒精灯等合理答案均给分
气球、酒精灯等合理答案均给分![]()
![]() 用硝酸银溶液滴定的过程中,由于Ag+优先与CN-反应,当滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失时,说明已经滴定到终点。根据化学计量关系可知
用硝酸银溶液滴定的过程中,由于Ag+优先与CN-反应,当滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失时,说明已经滴定到终点。根据化学计量关系可知![]() ,氰化钠的纯度为
,氰化钠的纯度为![]() ,故答案为:滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失;
,故答案为:滴入最后一滴硝酸银溶液时,溶液中出现淡黄色沉淀,且半分钟内沉淀不消失;![]() 或
或![]() 。
。