题目内容
3.已知如图转化关系中,甲、乙均为单质,下列判断正确的是( )
| A. | 甲可能是钠 | B. | 乙可能是氢气 | ||
| C. | 丙可能是氧化铝 | D. | 丙可能是三氧化硫 |
分析 A、钠和氯气点燃反应生成氯化钠,氯化钠溶于水得到氯化钠溶液,电解氯化钠溶液得到氢氧化钠、氢气和氯气;
B、乙为氢气,甲可以是非金属单质如氯气,氢气和氯气反应得到氯化氢气体,氯化氢气体溶于水得到盐酸,盐酸电解得到氢气和氯气;
C、丙为氧化铝,则甲乙为铝和氧气,氧化铝不溶于水;
D、丙若为三氧化硫,单质硫点燃不能生成三氧化硫.
解答 解:A、若甲为钠,结合关系分析,钠和氯气点燃反应生成氯化钠,氯化钠溶于水得到氯化钠溶液,电解氯化钠溶液得到氢氧化钠、氢气和氯气,不能得到钠和氯气,应是电解熔融氯化钠得到金属钠和氯气,故A错误;
B、乙为氢气,甲可以是非金属单质如氯气,氢气和氯气反应得到氯化氢气体,氯化氢气体溶于水得到盐酸,盐酸电解得到氢气和氯气,符合转化关系,故B正确;
C、丙为氧化铝,氧化铝不溶于水,不能实现上述转化,故C错误;
D、丙若为三氧化硫,单质硫点燃不能生成三氧化硫,只能生成二氧化硫,故D错误;
故选B.
点评 本题考查了元素化合物性质分析,物质转化关系的理解应用,主要是钠、硫、铝及其化合物性质的分析应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
14.铝热反应为放热反应.常温下,已知:4Al(s)+3O2(g)═2Al2O3(s)△H1,4Fe(s)+3O2(g)═2Fe2O3(s)△H2,下面关于△H1、△H2的比较正确的是( )
| A. | △H1>△H2 | B. | △H1<△H2 | C. | △H1=△H2 | D. | 无法判断 |
11. 甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.
(1)在25℃、101KPa下,1g甲醇(液态)燃烧生成CO2和液态水放热22.68kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol.(△H的数值保留小数点后1位)
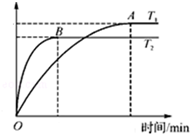
(2)工业上用CO与H2反应生成甲醇(催化剂为Cu2O/ZnO).一定条件下,在体积为3L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g).甲醇的物质的量随温度的变化如图所示,请回答下列问题:
①该反应正向为放热反应(填“放热”或“吸热”),升高温度,平衡常数K<(填“增大”、“减小”或“不变”).
②该反应的△S<0(填“>”或“<”)在较低(填“较高”或“较低”)温度下有利于该反应自发进行.
③温度为T2时,从反应开始到平衡,H2表示的平均反应速率v(H2)=$\frac{2nB}{3tB}$mol/(L.min).
④在其他条件不变的情况下,将处于C点的平衡体系体积压缩到原来的1/2,重新平衡时,下列有关该体系的说法正确的是BC.
A. H2的浓度减小 B.甲醇的百分含量增大 C.$\frac{c(C{H}_{3}OH)}{{c}^{2}({H}_{2})•c(CO)}$减小 D.$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大
(3)已知反应2CH3OH(g)═CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正> v逆(填“>”、“<”或“=”).
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L,该时间内反应速率v(CH3OH)=0.16mol/L.
 甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.(1)在25℃、101KPa下,1g甲醇(液态)燃烧生成CO2和液态水放热22.68kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol.(△H的数值保留小数点后1位)
(2)工业上用CO与H2反应生成甲醇(催化剂为Cu2O/ZnO).一定条件下,在体积为3L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g).甲醇的物质的量随温度的变化如图所示,请回答下列问题:
①该反应正向为放热反应(填“放热”或“吸热”),升高温度,平衡常数K<(填“增大”、“减小”或“不变”).
②该反应的△S<0(填“>”或“<”)在较低(填“较高”或“较低”)温度下有利于该反应自发进行.
③温度为T2时,从反应开始到平衡,H2表示的平均反应速率v(H2)=$\frac{2nB}{3tB}$mol/(L.min).
④在其他条件不变的情况下,将处于C点的平衡体系体积压缩到原来的1/2,重新平衡时,下列有关该体系的说法正确的是BC.
A. H2的浓度减小 B.甲醇的百分含量增大 C.$\frac{c(C{H}_{3}OH)}{{c}^{2}({H}_{2})•c(CO)}$减小 D.$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大
(3)已知反应2CH3OH(g)═CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L,该时间内反应速率v(CH3OH)=0.16mol/L.
18.下列反应对应的离子方程式正确的是( )
| A. | 等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| B. | 过氧化钠溶于水:2022-+2H2O=4OH-+O2↑ | |
| C. | 用MnO2从酸化的海带灰中浸取液中提取碘:MnO2+2I-+2H2O=Mn2++I2+4OH- | |
| D. | 向偏铝酸钠溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
15.下列反应的离子方程式书写正确的是( )
| A. | 将鸡蛋壳在醋酸中溶解有气泡产生:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 向硫酸铜溶液中加入氢氧化钡溶液:Cu2++2OH-═Cu(OH)2↓ | |
| C. | 将Cu丝插入AgNO3溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 向KHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:2H++SO${\;}_{4}^{2-}$+Ba2++2OH-═2H2O+BaSO4↓ |
12.用Na2CO3粉末配制1mol/L的Na2CO3100mL,配制中需用仪器的先后顺序是( )
①托盘天平 ②量筒 ③50mL烧杯 ④药匙 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
①托盘天平 ②量筒 ③50mL烧杯 ④药匙 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
| A. | ①③⑤⑥⑦ | B. | ④①③⑦⑤⑥ | C. | ④①⑤⑦⑥ | D. | ④②③⑦⑤⑥ |
13.下列关于平衡常数的说法中,正确的是( )
| A. | 化学平衡常数用来定量描述化学反应的限度 | |
| B. | 利用化学平衡常数判断化学反应进行的快慢 | |
| C. | 平衡常数的大小与温度、浓度、压强、催化剂有关 | |
| D. | 对于一个化学反应达到平衡之后,若只改变一个因素使得平衡发生移动,则K值一定变化 |